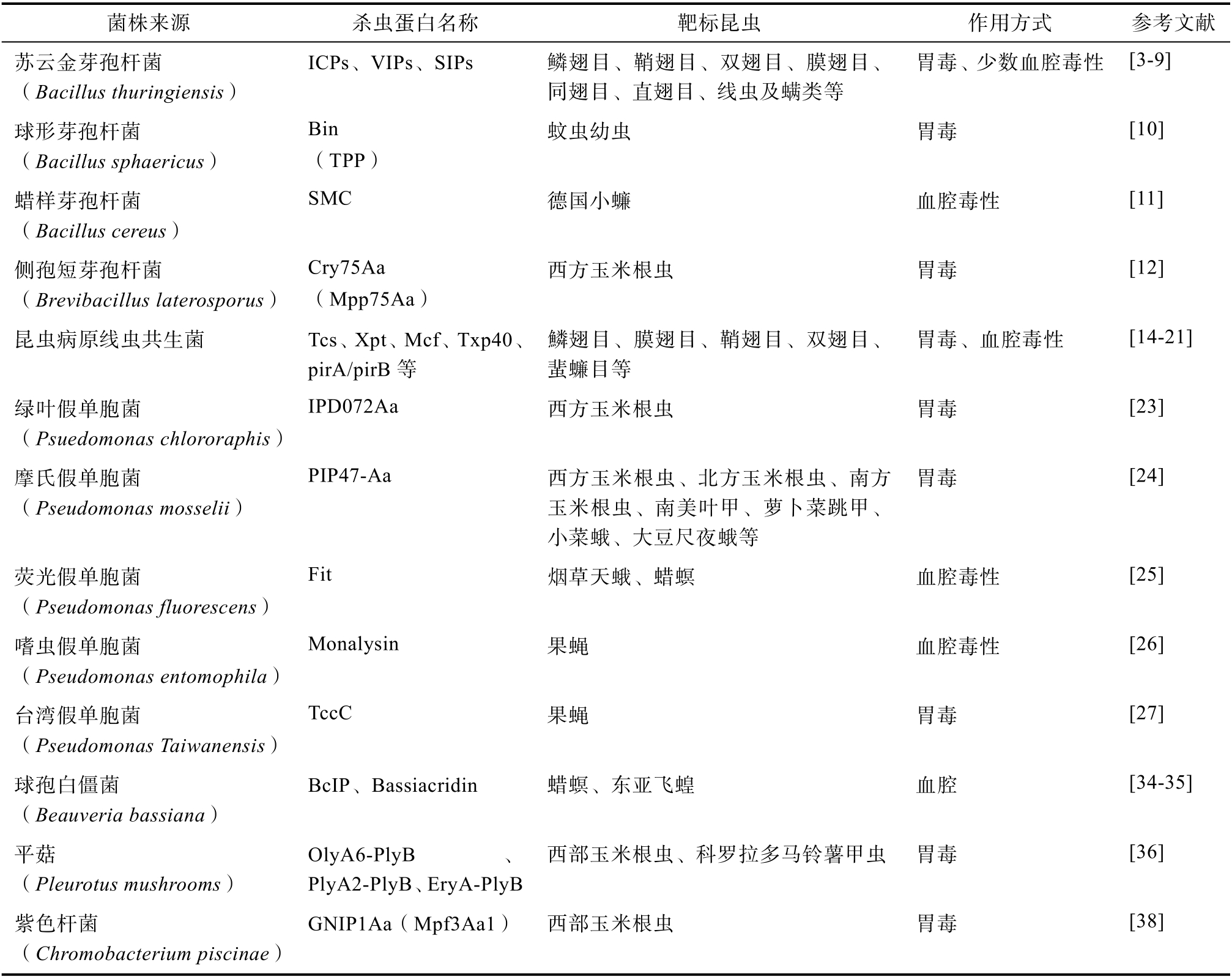
杀虫蛋白,是一类具有杀虫效果的蛋白质类物质。首次确定杀虫蛋白是在1953 年,Hannay 等通过研究发现,促使苏云金芽孢杆菌(Bacillus thuringiensis,Bt)发挥杀虫作用的物质主要是其产生的伴胞晶体,且证实这种伴胞晶体的本质就是蛋白质,由此杀虫蛋白走进公众视野。随着分子生物学的不断发展,1981 年,Schnepf 和Whiteley成功分离得到第一个来自于Bt 的杀虫蛋白基因cry,开创了杀虫蛋白在分子水平研究的新纪元。此后,越来越多的杀虫蛋白基因被挖掘,植物、动物、微生物中均被证实有杀虫蛋白的存在,其中微生物源杀虫蛋白种类最多,研究更深入[1]。本文对近年来发现的微生物源杀虫蛋白及其靶标昆虫和作用方式等信息进行汇总(表1),为后续相关研究提供便利。
表1 杀虫蛋白信息汇总表
Table 1 Summary of insecticidal proteins
菌株来源 杀虫蛋白名称 靶标昆虫 作用方式 参考文献苏云金芽孢杆菌(Bacillus thuringiensis)ICPs、VIPs、SIPs 鳞翅目、鞘翅目、双翅目、膜翅目、同翅目、直翅目、线虫及螨类等胃毒、少数血腔毒性 [3-9]球形芽孢杆菌(Bacillus sphaericus)Bin(TPP)蚊虫幼虫 胃毒 [10]蜡样芽孢杆菌(Bacillus cereus)SMC 德国小蠊 血腔毒性 [11]侧孢短芽孢杆菌(Brevibacillus laterosporus)Cry75Aa(Mpp75Aa)西方玉米根虫 胃毒 [12]昆虫病原线虫共生菌 Tcs、Xpt、Mcf、Txp40、pirA/pirB 等鱗翅目、膜翅目、鞘翅目、双翅目、蜚蠊目等胃毒、血腔毒性 [14-21]绿叶假单胞菌(Psuedomonas chlororaphis)IPD072Aa 西方玉米根虫 胃毒 [23]摩氏假单胞菌(Pseudomonas mosselii)PIP47-Aa 西方玉米根虫、北方玉米根虫、南方玉米根虫、南美叶甲、萝卜菜跳甲、小菜蛾、大豆尺夜蛾等胃毒 [24]荧光假单胞菌(Pseudomonas fluorescens)Fit 烟草天蛾、蜡螟 血腔毒性 [25]嗜虫假单胞菌(Pseudomonas entomophila)Monalysin 果蝇 血腔毒性 [26]台湾假单胞菌(Pseudomonas Taiwanensis)TccC 果蝇 胃毒 [27]球孢白僵菌(Beauveria bassiana)BcIP、Bassiacridin 蜡螟、东亚飞蝗 血腔 [34-35]平菇(Pleurotus mushrooms)OlyA6-PlyB 、PlyA2-PlyB、EryA-PlyB西部玉米根虫、科罗拉多马铃薯甲虫 胃毒 [36]紫色杆菌(Chromobacterium piscinae)GNIP1Aa(Mpf3Aa1) 西部玉米根虫 胃毒 [38]
1 微生物源杀虫蛋白
1.1 芽孢杆菌科(Bacillaceae)/类芽孢杆菌科(Paenibacillaceae)
芽孢杆菌,是一类能产生抗力内生孢子的革兰氏阳性菌。目前,来源于芽孢杆菌属的苏云金芽孢杆菌是农业生产中应用最广的微生物制剂,很多来源于Bt 的杀虫蛋白基因也已经被成功商业化应用[2]。Bt 杀虫蛋白分为杀虫晶体蛋白(insecticidal crystal proteins,ICPs)、营养期杀虫蛋白(vegetative insecticidal proteins,VIPs)和分泌型杀虫蛋白(secreted insecticidal protein,SIPs)。其中ICPs 是在释放芽孢时形成的,分为Cry 和Cyt 两类,对鳞翅目(Lepidoptera)、鞘翅目(Coleoptera)、双翅目(Diptera)、膜翅目(Hymenoptera)、同翅目(Homoptera)、直翅目(Orthoptera)、线虫(Nematode)及螨类(Mite)等都具有特异的杀虫活性[3-7]。VIPs,SIPs 则是在Bt 生长过程中产生的,对双翅目、鳞翅目、鞘翅目这几类昆虫具有杀虫特异性[8-9]。
除苏云金芽孢杆菌外,球形芽孢杆菌(Bacillus sphaericus)以其对蚊虫幼虫的高毒性而闻名,其产生的二元毒素Bin 毒素(TPP 蛋白),已被广泛用作灭蚊剂[10]。来自蜡样芽孢杆菌(Bacillus cereus)的天然sphingomyelinase C(SMC)蛋白及在大肠杆菌重组表达后都被发现可通过低剂量注射快速麻痹和杀死德国小蠊(Blattela germanica)[11]。David Bowen 等经研究确定了三种来自类芽孢杆菌科的侧孢短芽孢杆菌(Brevibacillus laterosporus)的新蛋白 Cry75Aa1(Mpp75Aa1)、Cry75Aa2(Mpp75Aa2)和Cry75Aa3(Mpp75Aa3)具有对西方玉米根虫(Diabrotica virgifera virgifera LeConte)的杀虫活性[12]。(类)芽孢杆菌科是目前发现杀虫蛋白种类最多,被业界认为最具有杀虫蛋白挖掘潜力的菌种。
1.2 昆虫病原线虫共生菌/ 肠杆菌科(Enterobacteriaceae)
昆虫病原线虫共生菌是一类与昆虫病原线虫(entomopathogenic nematodesm,EPNs)互惠共生的杆状细菌,属于肠杆菌科,主要包括致病杆菌属(Xenorhabdus)和发光杆菌属(Photorhabdus)。
1998 年, Bowen 等首次在发光杆菌(Photorhabdus luminescens)W14 发酵液中发现与苏云金芽孢杆菌杀虫晶体蛋白显现出类似杀虫活性和致病特征的Tcs 杀虫蛋白复合体,复合体由TcA(280 kDa)、TcB(170 kDa)、TcC(110 kDa)三种类型的功能蛋白组成[13],在喂食或注射的条件下对鱗翅目、膜翅目、鞘翅目、双翅目等多种害虫均具有毒杀作用[14-16]。而后,类似Tcs 复合体的蛋白也在其它昆虫病原线虫共生菌中被发现,如来自致病杆菌属细菌的Xpt(Xenorhabdus protein toxin)蛋白,来自嗜虫沙雷氏菌(Serratia entomophila)的Sep(Sentomophila pathogenicity)蛋白。2019 年,Mai Morishita 等从肠杆菌科细菌Enterobacter sp.532 菌株中分离到一种对家蚕具有致病性的蛋白itcA,因经鉴定是Tcs 复合体A组分的同源物,其VRP1 结构域是保守的,且在itcA 下游区域,还发现了Tcs 复合体B 和C 成分基因的同源物[17]。由此看来,Tc 蛋白在肠杆菌科中具有广谱性。
除TcS 外,发光杆菌中普遍存在的致软毒素Mcf(makes caterpillars floppy)能够促使烟草天蛾等蛾类幼虫的血细胞和中肠上皮细胞凋亡,同时破坏肠道,使昆虫渗透失调,最后瘫软死亡[18]。将Mcf 的C 端截短,保留N 端促细胞凋亡的BH3结构域,仍能对甜菜夜蛾幼虫表现出喂食毒性和血腔毒性[19],可见BH3 结构域是Mcf 发挥杀虫作用的重要功能区。发光杆菌中还有一种常见的二元杀虫蛋白 pirA/pirB(Photorhabdus Insect-Related,Pr)蛋白具有较强的昆虫口服和血腔毒性,孙建宇通过实验确定PirA2B2 蛋白对致倦库蚊(Culex quinquefasciatus)和白纹伊蚊(Aedes albopictus)有口服杀虫活性,对大蜡螟(Galleria mellonella)和斜纹夜蛾(Spodopteralitura Fabricius)5 龄幼虫、黄粉虫(Tenebrio molitor)、德国小蠊(Blattella germanica)具有一定的血腔杀虫活性,但当pirA2 和pirB2 基因单独表达时,对大蜡螟和斜纹夜蛾5 龄幼虫则不表现血腔活性[20]。Txp40(Toxin from Xenorhabdus and Photorhabdus,40kDa)是一种普遍存在于昆虫病原线虫共生菌致病杆菌属和发光杆菌属中的杀虫蛋白,在对棉铃虫(Helicoverpa armigera)的毒性研究中,Prakash Y 等分析Txp40 可能与棉铃虫中肠受体蛋白钙粘蛋白、ATP 结合盒、氨基肽酶N1 和碱性磷酸酶相互作用,从而产生毒性[21]。
昆虫病原线虫共生菌因其含有的杀虫蛋白种类之多,杀虫图谱之广,已被广泛认可为可替代Bt,用于新的转基因抗虫植物研究的潜力菌种。
1.3 假单胞菌科(Pseudomonadaceae)
假单胞菌是几乎无处不在的细菌,包括土壤、水和植物表面,是生防常用菌,具有杀虫、降解有毒物质等生物防治作用[22]。2016 年9 月,美国杜邦先锋公司报道,从绿叶假单胞菌(Psuedomonas chlororaphis)中发现IPD072Aa 蛋白对西方玉米根虫表现出杀虫能力,转ipd072Aa 基因的玉米可免受西方玉米根虫的危害,且经证实其重要农艺性状和营养成分可视为与常规玉米基本一样[23]。2021 年2 月9 日,澳新食品标准局(Food Standards Australia New Zealand,FSANZ)发布批准能同时表达DvSSJ1 双链RNA 和IPD072Aa 蛋白的耐除草剂和抗虫玉米品系DP23211 用于食品,这是非Bt 基因转基因作物的一次成功应用。2017 年6 月美国杜邦先锋公司再次报道了从摩氏假单胞菌(Pseudomonas mosselii)中发现了一个全新的杀虫蛋白PIP47-Aa,不存在任何已知的结构域和模体。该蛋白除了能够杀死西方玉米根虫外,还能够杀死鞘翅目北方玉米根虫(Diabrotica barberi)、南方玉米根虫(Diabrotica undecimpunctata howardi)、南美叶甲(Diabrotica speciosa)、萝卜菜跳甲(Phyllotreta cruciferae)及鳞翅目害虫小菜蛾(Plutella xylostella)、大豆尺夜蛾(Pseudoplusia includens)等,同时对益虫瓢虫无毒性[24]。杀虫谱更广、对非靶标昆虫无害、与已知杀虫蛋白无交互抗性成为了PIP47-Aa 杀虫蛋白的3 个突出优势。
此外,荧光假单胞菌(Pseudomonas fluorescens)的Fit 蛋白对烟草天蛾(Manduca sexta)和蜡螟具有毒杀活性[25]。嗜虫假单胞菌(Pseudomonas entomophila)的Monalysin 蛋白与来自台湾假单胞菌(Pseudomonas Taiwanensis)的TccC 杀虫蛋白等均表现出对果蝇(Drosophila)幼虫的毒性[26-27]。假单胞菌中杀虫蛋白的发现,证明在其它细菌源甚至是革兰氏阴性菌中寻找强力有效的杀虫蛋白是具有可能性的。
1.4 真菌(Fungi)
真菌是最早被发现可以作为防治害虫的微生物,当前已知的以昆虫为寄主的真菌超过750 种,涉及昆虫超过200 种[28]。其中,白僵菌和绿僵菌是在虫害防治中应用最广泛的虫生真菌,其主要代谢产物为破坏素(destruxins,dtxs),是由一个α-羟基酸和五个氨基酸残基组成的环六肽,可以抑制细胞和体液免疫反应,从而帮助真菌在昆虫中繁殖,达到毒杀目的[29]。王成树课题组通过比较产破坏素的金龟子绿僵菌(Metarhizium anisopliae)和不产破坏素的蝗绿僵菌(Metarhizium acri)的基因组信息,同时对靶向基因进行破坏确定了破坏素合成途径主要是由dtxS1、dtxS2、dtxS3、dtxS4四个基因编码调控,并经验证,绿僵菌突变菌ΔdtxS1 确实由于NRP 合成酶的缺失不能产生破坏素,改变杀虫活性[30]。该课题组还通过全基因组测序不同杀虫真菌以发掘杀虫毒力蛋白,分别证实缺失mast12、mpl1、mrVeA、mrVelB 等基因的绿僵菌突变体,会失去杀虫能力[31-33]。此外,在球孢白僵菌(Beauveria bassiana)培养液中也分离纯化出能够通过注射蜡螟引起细胞毒性及昆虫黑化反应的壳聚糖酶类似蛋白BcIP(Beauveria chitosanase-like protein)和对东亚飞蝗(Locnsta migratoria)具有专化性的注射毒性的Bassiacridin蛋白[34-35]。
近年来,大型食用真菌的活性成分在生物源杀虫剂方面的开发也逐步受到重视,如平菇(Pleurotus mushrooms)中的溶血素家族蛋白OlyA6(ostreolysin A6),PlyA2(pleurotolysin A2)和 EryA(erylysin A)会与蛋白伴侣 PlyB(pleurotolysin B)结合,协同作用于磷酸乙醇胺神经酰胺(ceramide phosphoethanolamine,CPE)和跨膜孔的形成,蛋白与蛋白伴侣形成的复合物对西方玉米根虫幼虫、成虫和科罗拉多马铃薯甲虫(Leptinotarsa decemlineata)幼虫表现出选择性毒性。同时,由于它们是与受体相互作用,因此进化出抗性的机会应较小[36]。此外,真菌酶系丰富,分泌的蛋白酶、几丁质酶和脂酶等能够降解害虫体壁从而达到杀虫效果,但这些酶的经口毒性还有待研究[37]。
1.5 其他
除上述来源分类,还有其它来自细菌的杀虫蛋白,如紫色杆菌(Chromobacterium piscinae)中发现的革兰氏阴性杀虫蛋白GNIP1Aa(Mpf3Aa1)不仅对西方玉米根虫表现出特异性的杀虫活性,且经过序列分析未发现与任何已知的杀虫蛋白具有同源性,这表明该蛋白可能是以一种新的方式杀灭WCR,为今后杀虫蛋白的应用提供了更多的可能性[38]。
其实,随着基因组测序项目的不断增加,以及蛋白质结构预测方法的不断改进,人们发现,细菌产生杀虫蛋白的范围越来越广,苏云金芽孢杆菌早已不再是杀虫蛋白的唯一来源。2020 年,国际杀虫蛋白命名委员会就以1998 年苏云金芽孢杆菌蛋白命名规则为基础[39],根据蛋白结构及保守结构域对蛋白序列重新进行分组,并更新了命名方式。修订后的命名信息可通过细菌杀虫蛋白资源中心网站(BPPRC,https://www.bpprc.org/)进行搜索,该资源中心网站上的信息显示,截至2021 年5 月,细菌杀虫蛋白有App、Cry、Cyt、Gpp、Mcf、Mpf、Mpp、Mtx、Pra、Prb、Spp、Tpp、Vip、Vpa、Vpb、Xpp 十六大类,共1 047种[40]。当然,这个数据还会不断被更新。
2 讨论与展望
虫害严重制约着农林业的发展,据农业部统计,农药的施用可减少因虫害造成的经济损失约300 亿元[41],但化学农药的长期施用不仅使害虫抗性提高,而且对环境造成污染,因此开发环境友好的新型生物农药已成为必然趋势。杀虫蛋白作为一种优质的生物防治剂,同化学农药相比,具有安全性高、对环境友好、不易产生抗药性等优点,同其它生物农药如:昆虫信息素、植物源杀虫剂及微生物源菌剂相比,又具有来源广泛、作用位点独特、重组蛋白获取成本低等特点,在虫害防治上已逐渐成为新的技术储备和其它农药的有力补充。但目前也存在亟待解决的问题,实际防治应用中只以苏云金芽孢杆菌为主,长期大面积连续种植Bt 转基因作物以及单一使用Bt 菌剂,缺乏多样性,导致昆虫抗性日益严重。所以,对微生物源除苏云金芽孢杆菌外的细菌及杀虫真菌,乃至植物源和动物源的杀虫蛋白基因的发掘将是至关重要的。
另一方面,由于蛋白类物质较化合物类药剂在结构稳定性上存在劣势,在开放环境中的应用受到限制,目前主要以转基因作物的形式实现其虫害防治功能。若能通过基因工程和蛋白质工程的手段,提升杀虫蛋白质的稳定性,便可为生物药剂形式的应用提供可能。这不仅可以缓解民众对转基因作物的排斥心理,同时还能为将来与其它生物药剂进行复配,对害虫进行多靶点消灭打下坚实的基础,最终实现综合防治。
[1] HARITH FADZILAH N, ABDUL-GHANI I, HASSAN M.Proteomics as a tool for tapping potential of entomopathogens as microbial insecticides[J]. Arch Insect Biochem Physiol, 2019,100(1): e21520. doi: 10.1002/arch.21520.
[2] AZIZOGLU U, JOUZANI G S, YILMAZ N, et al. Genetically modified entomopathogenic bacteria, recent developments, benefits and impacts: A review[J]. Science of The Total Environment,2020, 734: 139169. doi: 10. 1016/j.scitotenv.2020.139169.
[3] ZHONG Y, AHMED S, DENG G, et al. Improved insect resistance against Spodoptera litura in transgenic sweetpotato by overexpressing Cry1Aa toxin[J]. Plant Cell Rep, 2019, 38(11):1439-1448. doi: 10. 1007/s00299-019-02460-8.
[4] BERRETTA M F, PEDARROS A S, SAUKA D H, et al.Susceptibility of agricultural pests of regional importance in South America to a Bacillus thuringiensis Cry1Ia protein[J]. J Invertebr Pathol, 2020, 172: 107354. doi: 10.1016/j.jip.2020.107354.
[5] LOTH K, COSTECHAREYRE D, EFFANTIN G, et al. New Cyt-like δ-endotoxins from Dickeya dadantii: structure and aphicidal activity[J]. Sci Rep, 2015, 5: 8791. doi: 10.1038/srep08791.
[6] VALTIERRA-DE-LUIS D, VILLANUEVA M, LAI L, et al.Potential of Cry10Aa and Cyt2Ba, two minority δ-endotoxins produced by Bacillus thuringiensis ser. israelensis, for the control of Aedes aegypti Larvae[J]. Toxins (Basel), 2020, 12(6):355. doi: 10.3390/toxins12060355.
[7] MEISSLE M, ROMEIS J. Transfer of Cry1Ac and Cry2Ab proteins from genetically engineered Bt cotton to herbivores and predators[J]. Insect Sci, 2018, 25(5): 823-832. doi: 10.1111/1744-7917.12468.
[8] SYED T, ASKARI M, MENG Z, et al. Current insights on vegetative insecticidal proteins (Vip) as next generation pest killers[J]. Toxins (Basel), 2020, 12(8): 522. doi: 10.3390/toxins12080522.
[9] WANG J, DING M Y, WANG J, et al. In silico Structure-based investigation of key residues of insecticidal activity of Sip1Aa protein[J]. Front Microbiol, 2020, 11: 984. doi: 10.3389/fmicb.2020.00984.
[10] PARK H W, BIDESHI D K, FEDERICI B A. Properties and applied use of the mosquitocidal bacterium, Bacillus sphaericus[J]. J Asia Pac Entomol, 2010, 13(3): 159-168. doi: 10.1016/j.aspen.2010.03.002.
[11] NISHIWAKI H, ITO K, OTSUKI K, et al. Purification and functional characterization of insecticidal sphingomyelinase C produced by Bacillus cereus[J]. Eur J Biochem, 2004, 271(3):601-606. doi: 10.1111/j.1432-1033.2003.03962.x.
[12] BOWEN D, YIN Y, FLASINSKI S, et al. Cry75Aa (Mpp75Aa)insecticidal proteins for controlling the western corn rootworm,Diabrotica virgifera virgifera, (Coleoptera: Chrysomelidae),isolated from the insect pathogenic bacteria Brevibacillus laterosporus[J]. Appl Environ Microbiol, 2020, 87(5): e02507-20. doi: 10.1128/AEM.02507-20.
[13] FFRENCH-CONSTANT R, WATERFIELD N. An ABC guide to the bacterial toxin complexes[J]. Adv Appl Microbiol, 2006, 58:169-183.
[14] SANTHOSHKUMAR K, MATHUR C, MANDAL A, et al. A toxin complex protein from Photorhabdus akhurstii conferred oral insecticidal activity against Galleria mellonella by targeting the midgut epithelium[J]. Microbiol Res, 2021, 242: 126642.doi: 10.1016/j.micres.2020.126642.
[15] MATHUR C, PHANI V, KUSHWAH J, et al. TcaB, an insecticidal protein from Photorhabdus akhurstii causes cytotoxicity in the greater wax moth, Galleria mellonella[J]. Pestic Biochem Physiol, 2019, 157: 219-229. doi: 10.1016/j.pestbp.2019.03.019.
[16] DA-SILVA W J, PILZ-JÚNIOR H L, HEERMANN R, et al. The great potential of entomopathogenic bacteria Xenorhabdus and Photorhabdus for mosquito control: a review[J]. Parasit Vectors,2020, 13(1): 376. doi: 10.1186/s13071-020-04236-6.
[17] MORISHITA M, MASUDA A, MON H, et al. Identification of an insecticidal toxin produced by Enterobacter sp. strain 532 isolated from diseased Bombyx mori silkworms[J]. FEMS Microbiol Lett, 2019, 366(2). doi: 10.1093/femsle/fny295.
[18] DABORN P J, WATERFIELD N, SILVA C P, et al. A single Photorhabdus gene, makes caterpillars floppy (mcf), allows Escherichia coli to persist within and kill insects[J]. Proc Natl Acad Sci USA, 2002, 99(16): 10742-10747. doi:10.1073/pnas.102068099.
[19] 谭思维. 发光杆菌mcf 杀虫基因的克隆和功能研究[D]. 湖南师范大学, 2009.TAN S W. Gene cloning and function study of mcf insecticidal gene from Photorhabdus luminescens[D]. Hunan Normal University,2009.
[20] 孙建宇. 荧光发光杆菌TT01 菌株pirAB 基因的克隆表达及杀虫谱研究[D]. 中山大学, 2012.SUN J Y. Cloning, Expression and insecticidal spectrum analysis of the pirAB gene from Photorhabdus Luminescens TT01[D].Sun Yat-sen University, 2012.
[21] SHANKHU P Y, MATHUR C, MANDAL A, et al. Txp40, a protein from Photorhabdus akhurstii, conferred potent insecticidal activity against the larvae of Helicoverpa armigera,Spodopteralitura and S. exigua[J]. Pest Manag Sci, 2020, 76(6):2004-2014. doi: 10.1002/ps.5732.
[22] TEOH M C, FURUSAWA G, VEERA-SINGHAM G. Multifaceted interactions between the pseudomonads and insects: mechanisms and prospects[J]. Arch Microbiol, 2021, 203(5): 1891-1915. doi:10.1007/s00203-021-02230-9.
[23] SCHELLENBERGER U, ORAL J, ROSEN B A, et al. A selective insecticidal protein from Pseudomonas for controlling corn rootworms[J]. Science, 2016, 354(6312): 634-637. doi:10.1126/science.aaf6056.
[24] WEI J Z, O'REAR J, SCHELLENBERGER U, et al. A selective insecticidal protein from Pseudomonas mosselii for corn rootworm control[J]. Plant Biotechnol J, 2018, 16(2): 649-659.doi: 10.1111/pbi.12806.
[25] PÉCHY-TARR M, BRUCK D J, MAURHOFER M, et al.Molecular analysis of a novel gene cluster encoding an insect toxin in plant-associated strains of Pseudomonas fluorescens[J].Environ Microbiol, 2008, 10(9): 2368-2386. doi: 10.1111/j.1462-2920.2008.01662.x.
[26] NONAKA S, SALIM E, KAMIYA K, et al. Molecular and functional analysis of pore-forming toxin monalysin from entomopathogenic bacterium Pseudomonas entomophila[J].Front Immunol, 2020, 11: 520. doi: 10.3389/fimmu.2020.00520.
[27] LIU J R, LIN Y D, CHANG S T, et al. Molecular cloning and characterization of an insecticidal toxin from Pseudomonas taiwanensis[J]. J Agric Food Chem, 2010, 58(23): 12343-12349.doi: 10.1021/jf103604r.
[28] 亓兰达, 魏鹏霖, 张晗星, 等. 后基因组时代害虫生防真菌次级代谢产物的研究进展[J]. 中国科学: 生命科学, 2020, 50(6):589-598.QI L D, WEI P L, ZHANG H X, et al. Research progress on secondary metabolites of pest biocontrol fungi in post-genomic era[J]. SCIENTIA SINICA Vitae, 2020, 50(6): 589-598.
[29] LIU B L, TZENG Y M. Development and applications of destruxins: a review[J]. Biotechnol Adv, 2012, 30(6): 1242-1254.doi: 10. 1016/j. biotechadv.2011.10.006.
[30] WANG B, KANG Q, LU Y, et al. Unveiling the biosynthetic puzzle of destruxins in Metarhizium species[J]. Proc Natl Acad Sci USA, 2012, 109(4): 1287-1292. doi: 10.1073/pnas.1115983109.
[31] 黄威, 商艳芳, 高强, 等. 金龟子绿僵菌转录因子Mast12 调控真菌穿透能力及杀虫毒[C]. 2012 年中国菌物学会学术年会会议摘要. 中国: 中国菌物学会, 2012: 148-149.HANG W, SHANG Y F, GAO Q, et al. Transcription factor Mast12 regulates insect cuticle penetration and virulence in the entomopathogenic fungus Metarhizium anisopliae[C]. 2012 Chinese Society of Mycology Annual Conference Abstract.China: Chinese Society of Mycology, 2012: 148-149.
[32] 段志兵, 王兵, 高强, 等. 金龟子绿僵菌脂被蛋白MPL1 基因进化及其磷酸化位点突变的研究[C]. 中国菌物学会学术年会论文摘要集. 中国: 中国菌物学会, 2010: 222-224.DUAN Z B, WANG B, GAO Q, et al. Gene evolution and the phosohoyrlation site mutation sudies of a PeriliPin MPL1 in the inseet-pathogenic fungus Metarhizium anisopliae[C]. Chinese Society of Mycology Annual Meeting papers abstracts. China:Chinese Society of Mycology, 2010: 222-224.
[33] 唐桂容, 周俊花, 王成树. 罗伯茨绿僵菌Velvet 家族基因的功能研究[C]. 多彩菌物 美丽中国——中国菌物学会2019 年学术年会论文摘要. 中国: 中国菌物学会, 2019: 182.TANG G R, ZHOU J H, WANG C S. Functional study of the Velvet family genes of Metarhizium Roberts[C]. Colorful Fungi Beautiful China 2019 Annual Conference of Chinese Mycology Society Abstract. China: Chinese Society of Mycology, 2019:182.
[34] FUGUET R, THÉRAUD M, VEY A. Production in vitro of toxic macromolecules by strains of Beauveria bassiana, and purification of a chitosanase-like protein secreted by a melanizing isolate[J].Comp Biochem Physiol C Toxicol Pharmacol, 2004, 138(2):149-161. doi: 10.1016/j.cca.2004.06.009.
[35] QUESADA-MORAGA E, VEY A. Bassiacridin, a protein toxic for locusts secreted by the entomopathogenic fungus Beauveria bassiana[J]. Mycol Res, 2004, 108(4): 441-452. doi: 10.1017/s0953756204009724.
[36] PANEVSKA A, HODNIK V, SKOČAJ M, et al. Pore-forming protein complexes from Pleurotus mushrooms kill western corn rootworm and Colorado potato beetle through targeting membrane ceramide phosphoethanolamine[J]. Sci Rep, 2019, 9(1): 5073.doi: 10.1038/s41598-019-41450-4.
[37] OLOMBRADA M, LÁZARO-GORINES R, LÓPEZ-RODRÍGUEZ J C, et al. Fungal ribotoxins: A review of potential biotechnological applications[J]. Toxins (Basel), 2017, 9(2): 71. doi: 10.3390/toxins9020071.
[38] SAMPSON K, ZAITSEVA J, STAUFFER M, et al. Discovery of a novel insecticidal protein from Chromobacterium piscinae,with activity against Western Corn Rootworm, Diabrotica virgifera virgifera[J]. J Invertebr Pathol, 2017, 142: 34-43. doi:10.1016/j.jip.2016.10.004.
[39] CRICKMORE N, ZEIGLER D R, FEITELSON J, et al.Revision of the nomenclature for the Bacillus thuringiensis pesticidal crystal proteins[J]. Microbiol Mol Biol Rev, 1998,62(3): 807-813.
[40] CRICKMORE N, BERRY C, PANNEERSELVAM S, et al. A structure-based nomenclature for Bacillus thuringiensis and other bacteria-derived pesticidal proteins[J]. J Invertebr Pathol,2020: 107438. doi: 10.1016/j.jip.2020.107438.
[41] 吴晓丽. 植物病害绿色防控大势所趋[J]. 科技导报, 2014,32(12): 2.WU X L. Green prevention and control of plant diseases is an irresistible trend[J]. Science & Technology Review, 2014,32(12): 2.