镉是一种毒性较强的重金属元素,能通过食物链进入人体并在体内富集,导致慢性中毒,损伤肝、肾等器官,引起“痛痛病”、慢性肾功能衰竭等疾病。根据GB 2762—2017[1],我国镉的限量标准为:谷物(稻谷除外)、谷物碾磨加工品(糙米、大米除外)≤0.1 mg/kg,稻谷、糙米、大米≤0.2 mg/kg。近年来,山东等多地发布了储备粮质量安全管理、超标粮食收购处置等制度,对粮食污染风险监测、储备粮出入库食品安全指标检测提出了明确要求。如何快速、准确地对大批量样品进行检测,成为粮食质检机构新的挑战。针对镉的检测,GB 5009.15—2014[2]规定了镉的石墨炉原子吸收光谱测定方法,并提供了四种前处理方法,其中压力消解罐消解法、湿式消解法、干法灰化法都存在操作繁琐、耗时长、用酸量大等弊端,干法灰化法还存在回收率偏低的问题,微波消解法是目前实验室用得较多的前处理方法,其优点是消解完全、准确性高,但也存在步骤繁琐、耗时长、用酸量大、消解罐价格昂贵等问题,极大地降低了消解效率。因此,开发快速、准确的前处理方法和定量方法成为提高重金属检测效率的首选。近几年,有采用不完全消解、快速消解等方法进行粮食中镉测定的研究[3-6],但存在以下有待完善之处:处理粮食品种单一,未对多种不同基质粮食样品进行消解研究;仅对标准物质样品进行试验,未对真实阳性样品进行研究;采用外标法定量分析,因标准溶液与样品溶液基体不匹配造成结果偏差;未进行样品量与酸量的比例优化;未与标准方法进行有效的结果比对等。针对上述问题,本文建立了基于GFAAS 的快速消解-标准加入法测定粮食中镉的方法,在现有研究的基础上,丰富了粮食基质类型,以我国三大粮食品种小麦、稻谷、玉米及主食大米作为研究对象,优化了快速消解前处理条件和步骤,确定了样品与硝酸最佳比例,探索了标准加入法在不同粮食基质下检测的准确性,并与GB 5009.15—2014 中微波消解法进行了全面比较,为粮食中镉的测定提供了可选的快速处理、准确定量方法。
1 材料与方法
1.1 实验材料
AA600 原子吸收光谱仪,配备横向加热石墨炉:美国珀金埃尔默公司;ETHOS UP 微波消解仪:意大利迈尔斯通公司;GSN-48 石墨赶酸器:基创仪器;GL124-1SCN 电子分析天平:赛多利斯公司;ADW-2002-M 超纯水系统:重庆颐洋;JXFM110 锤式旋风磨:上海嘉定粮油;50 mLPP刻度离心管:广州洁特。
GBW(E)080119 镉单元素溶液标准物质(100 µg/mL),使用前用1%硝酸进行逐级稀释,得到2 µg/L 上机标准溶液母液:中国计量科学院;硝酸(UP 级):苏州晶瑞;硝酸钯(10 000 mg/L),使用时稀释10 倍:美国珀金埃尔默公司。
GBW(E)100377 糙米粉标准物质、GBW(E)100380 玉米粉标准物质、GBW(E)100379 全麦粉标准物质:国家粮食和物资储备局科学研究院;GBW(E)100348a 大米粉标准物质:钢研纳克检测技术股份有限公司。
稻谷样品273#、玉米样品212#,小麦样品183#、大米样品166#、178#:本课题组采集。将稻谷脱壳后制成糙米273#,以上样品分别用锤式旋风磨制备成糙米粉、玉米粉、全麦粉、大米粉。
1.2 实验方法
1.2.1 快速消解前处理方法
称取0.3 g(精确到0.1 mg)样品,置于50 mL刻度离心管中,准确加入2.0 mL 硝酸,盖子旋转至适中松紧度(利于烟气散发,防止管内压力过大,同时避免硝酸快速蒸发而损失),将离心管置于石墨赶酸器中,120 ℃,消解15 min,取下并开盖放置10 min,待黄烟散尽并冷却后,用纯水定容至25 mL(可根据样品含量调整定容体积)。
1.2.2 标准曲线制作
采用标准加入法制作标准曲线。按照样品基质不同,分为糙米组、玉米组、小麦组、大米组,分组进行标准曲线制作。按照不同的组别,将所处理的单一粮种样品各吸取1 mL 进行混合,作为加标基质,记为Mix,标准空白为试剂空白,标准点进样程序见表1。样品进样程序:吸取16 µL样品、16 µL 稀释液(纯水)及5 µL 基体改进剂硝酸钯,总进样体积为37 µL。
表1 标准点进样程序
Table 1 Sample injection program of calibration point µL

标准点 稀释液 基体改进剂 上机母液 Mix 0 16 5 0 16标准点1 12 5 4 16标准点2 8 5 8 16标准点3 4 5 12 16标准点4 0 5 16 16
1.2.3 微波消解前处理方法
称取0.3 g(精确到0.1 mg)样品,置于消解罐中,准确加入8.0 mL 硝酸(国家标准方法为加入5 mL 硝酸和2 mL 过氧化氢,本研究根据微波消解仪使用方法推荐加入8 mL 硝酸,经前期比对,消解效果无显著差异),旋紧盖子,置于微波消解仪中,按照仪器运行程序消解52 min,通风降温30 min,温度降至50 ℃以下时,开罐,置于石墨赶酸器上,于160 ℃赶酸,约120 min 至近干,冷却后转移至10 mL 容量瓶中,用纯水定容。微波消解程序见表2。
表2 微波消解程序
Table 2 Program of microwave digestion
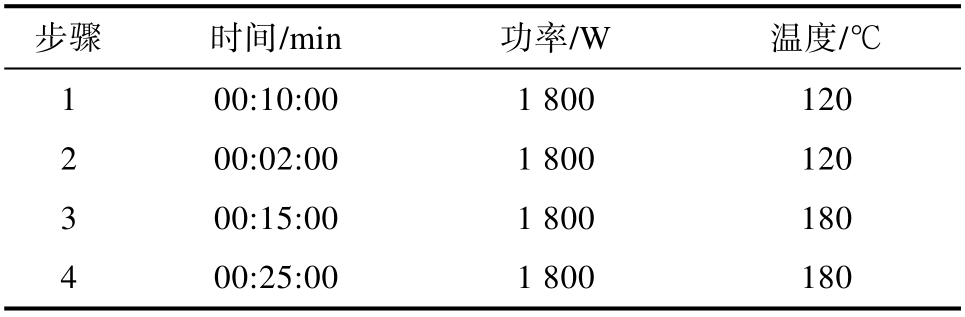
步骤 时间/min 功率/W 温度/℃1 00:10:00 1 800 120 2 00:02:00 1 800 120 3 00:15:00 1 800 180 4 00:25:00 1 800 180
1.2.4 仪器工作条件
石墨炉原子吸收光谱仪:测定波长228.8 nm,灯类型:HCL,灯电流4.0 mA,狭缝0.7 nm,纵向交流塞曼背景校正,升温程序见表3。
表3 石墨炉升温程序
Table 3 Temperature-rising program of graphite furnace

步骤 温度/℃ 爬升时间/s 保留时间/s 内部流量/(mL/min)1 120 5 30 250 2 170 20 30 250 3 500 10 30 250 4 1 600 0 5 0 5 2 450 1 3 250
1.3 数据分析
数据处理按照GB/T 4889—2008《数据的统计和解释正态分布均值和方差的估计与检验》[7],其中,方差一致性检验即F 检验按照“两总体方差或标准差比较的检验”规定的方法进行,两总体均值的比较检验即差异显著性检验按照附录B使用P 值进行假设检验。
2 结果与分析
2.1 方法条件的确定
2.1.1 硝酸浓度、用量及样品粒径选择
有研究显示采用稀酸作为提取液收到了良好效果[8-9],本研究为了确保消解效率,尽最大可能消解带种皮粮食样品中的复杂有机物,采用了68%硝酸作为消解液。采用了2 mL 硝酸加入量,在消解结束后,酸剩余量约为1~1.5 mL,定容到25 mL后,样品溶液酸度小于5%。在样品粒径选择上,试验了锤式旋风磨的粉碎效果,得到的粉样基本通过40 目筛(粒径约0.5 mm),试验结果显示,粒径为0.5 mm 粮食样品可以获得理想的消解效果。
2.1.2 样品与硝酸比例优化
考察了样品量与酸量最佳比例,以玉米粉标准物质(标准值为0.045 mg/kg)为消解样品,考察在0.3、0.4、0.5、0.6、1.0 g 称样量时的回收率,每组消解样品7 份,每份重复测定3 次,结果见图1。当固定酸量为2.0 mL 时,随着称样量增加,镉回收率逐渐降低。称样量为0.3~0.5 g 时,回收率>90%,符合该浓度水平回收率要求。当α= 0.05时,对5 组回收率进行F 检验,并利用P 值进行差异显著性检验。5 组回收率的精密度一致,称样量为0.3、0.4 g 时,两组回收率均值无显著性差异(F =1.02,F0.95(6,6) =4.28,F < F0.95(6,6);t=1.660,P=0.12,P>0.05)。称样量为0.3、0.5 g 时,两组回收率均值具有显著性差异(F =1.17,F0.95(6,6) =4.28,F < F0.95(6,6);t=4.788,P=0.000 4,P<0.05),以此确定样品与硝酸比例为0.3~0.4 g:2.0 mL。
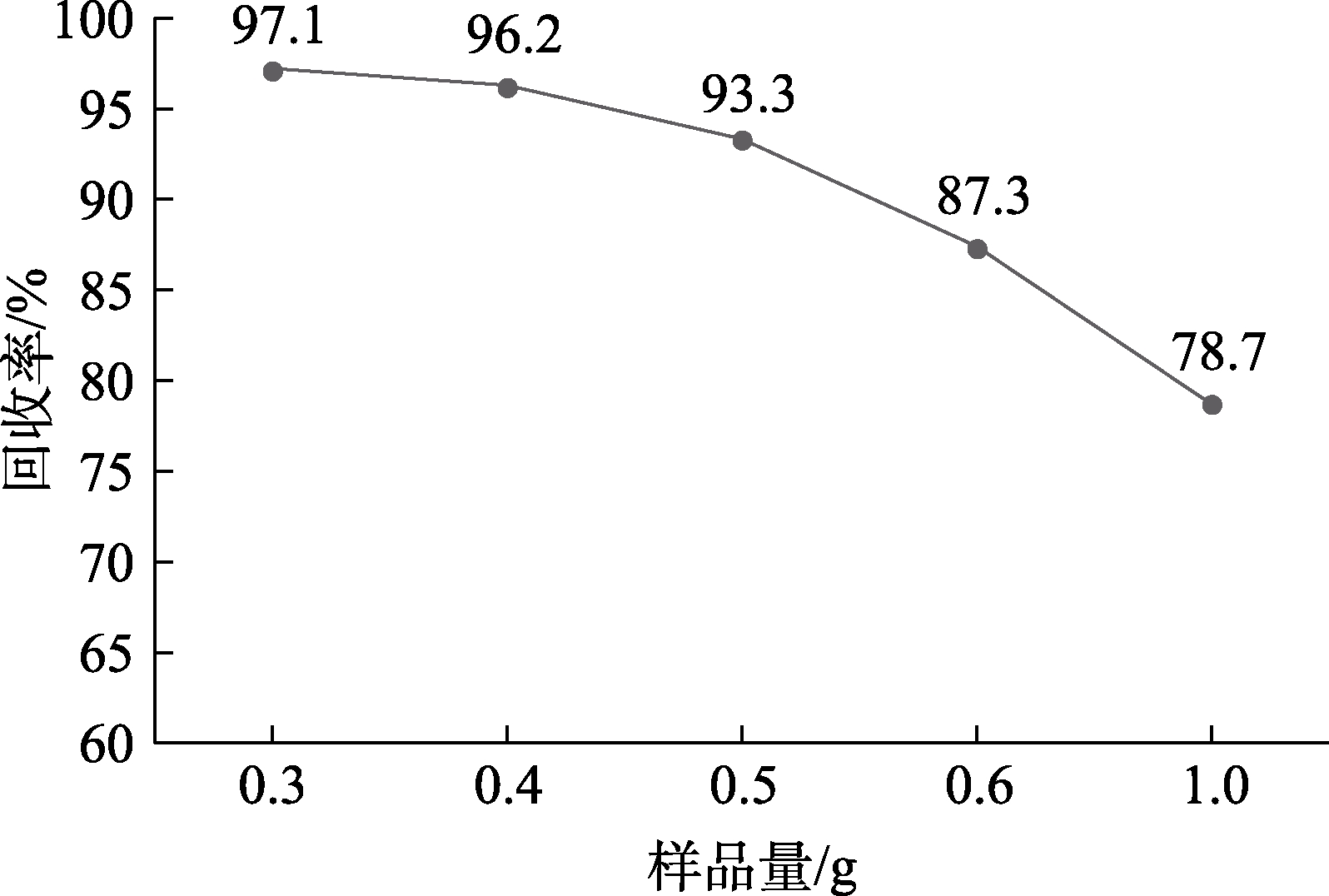
图1 不同样品量镉的回收率(n=7)
Fig.1 Recoveries of cadmium of different sample amounts (n=7)
2.1.3 消解温度、时间的确定
消解温度采用硝酸沸点120 ℃,比低温消解用时更少,消解效果更好。通过比较不同加热时间的消解效果发现,消解10 min 时溶液中有明显颗粒物,消解15 min 时,颗粒物基本消失且溶液呈透明状,20、25 min 后,无明显变化,因此确定消解时间为15 min。定容后大米粉样品呈近乎无色的均一溶液,糙米粉、玉米粉、全麦粉为淡黄色液体,有细小悬浮颗粒。
2.1.4 悬浮颗粒对测定结果的影响
消解了14 份全麦粉样品进行比对,其中7 份离心(6 000 r/min,10 min)后取上清液测定,7份直接上机测定,每份重复测定3 次,当α=0.05时,结果显示两组方差相等(F =3.13,F0.95(6,6) =4.28,F < F0.95(6,6)),均值无显著性差异(t=0.140,P=0.89,P>0.05),说明离心与不离心效果无明显差别,残留颗粒不影响测定,为减少操作环节,本方法采用定容后静置再进行上机测定。
2.2 方法线性
2.2.1 标准加入法的设置
为减少背景值对检测结果的影响,使标准溶液与样品溶液基体相匹配,本研究采用1.2.2 作为定量方法,将加标基质Mix 中待测元素含量记为CX,吸光度值记为AX,以加入待测元素镉的标准浓度(C1、C2、C3、C4)为横坐标,以相应吸光度分别减去样品Mix 吸光度的值为纵坐标(A1-AX,A2-AX,A3-AX,A4-AX),制作标准曲线。根据试验结果,镉浓度在0~5 µg/L 时线性良好,设0、0.5、1.0、1.5、2.0 µg/L 作为标准加入法的标准点。
2.2.2 不同基质的标准曲线相关系数r
考虑到不同样品消解后的基质存在差异,测定曲长228.8 nm 下,对不同的样品分别绘制标准曲线(以糙米为例,见图2),来验证不同基质下标准曲线的线性,并在不同时间进行了10 次试验以考察线性的稳定性。根据结果(图3),4 种基质的标准曲线相关系数均达到了0.995(0.998 占比最大),符合相关系数要求,表明标准加入法线性关系良好,且在4 种基质中都有良好的适应性和稳定性。
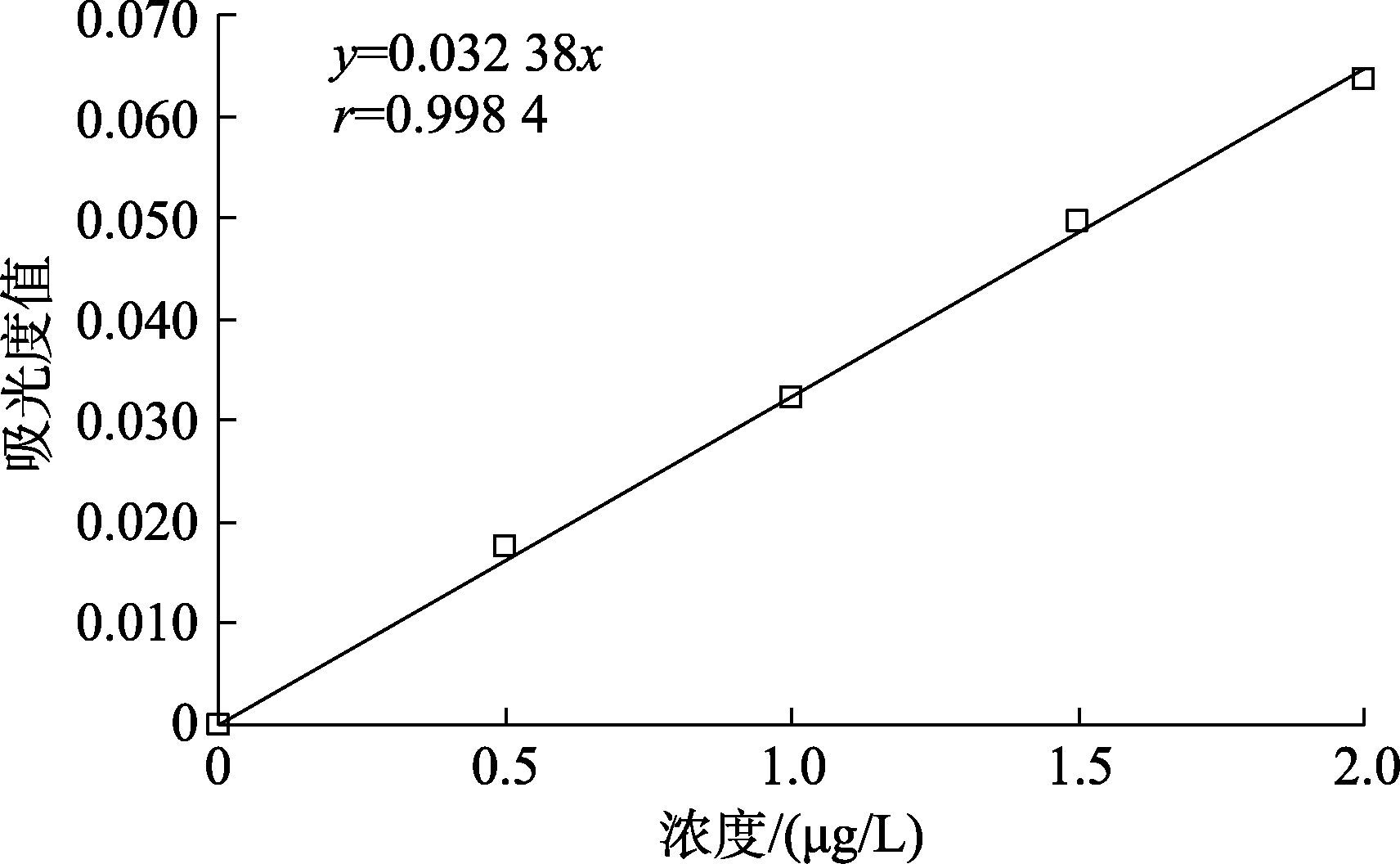
图2 糙米标准加入法标准曲线
Fig.2 Standard addition calibration curve of brown rice
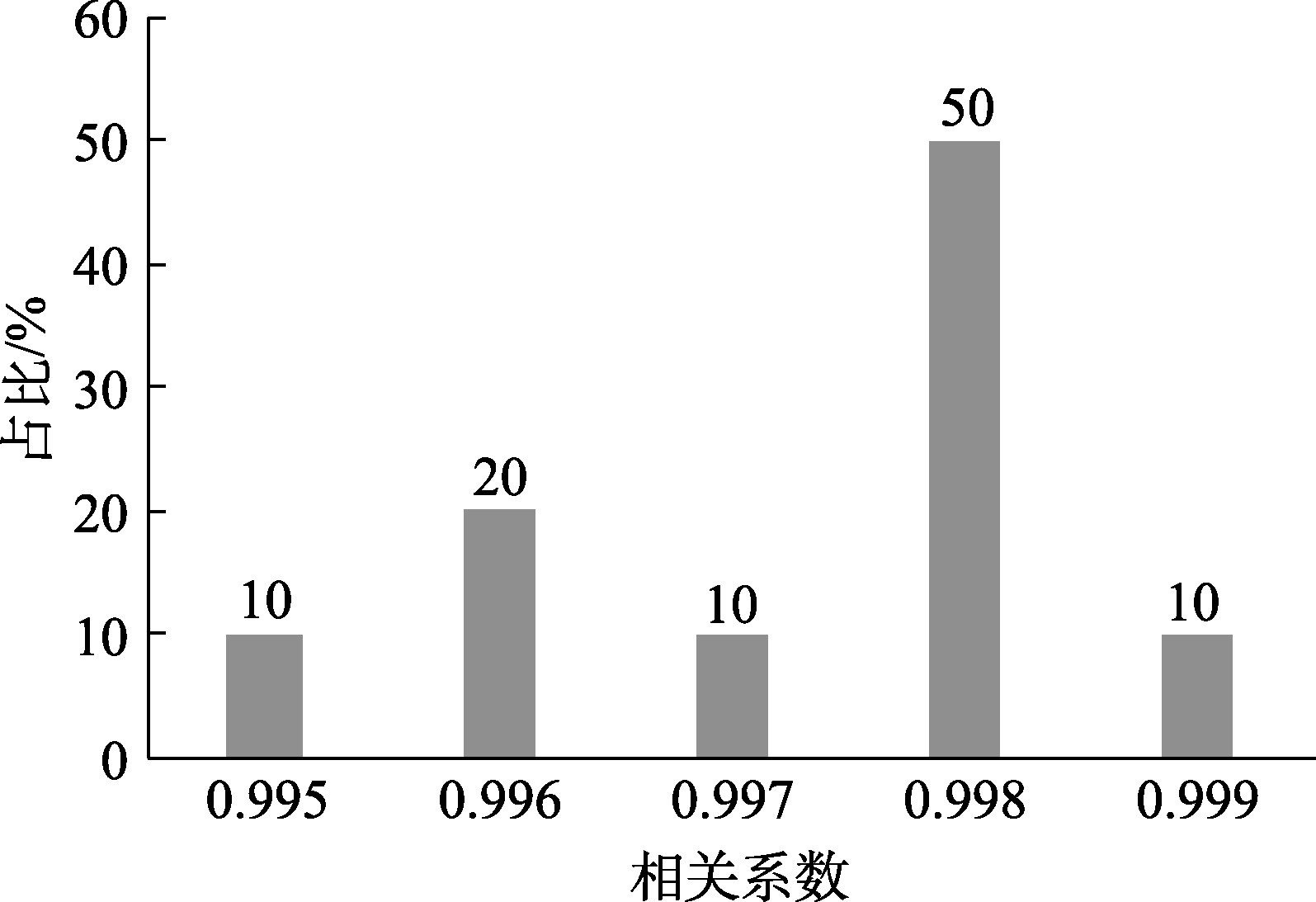
图3 相关系数占比
Fig.3 Proportion of correlation coefficients
2.3 方法准确度研究
2.3.1 有证标准物质(CRM)检测
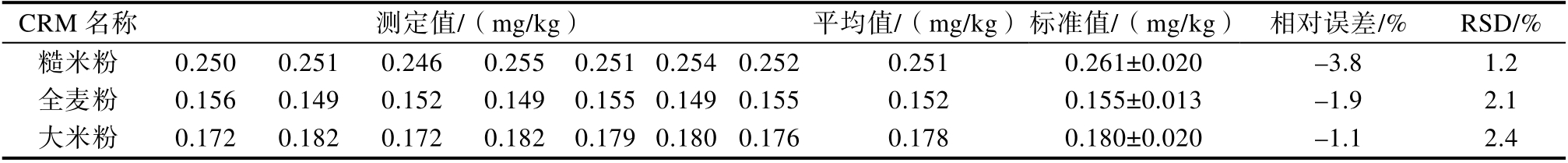
使用3 种不同基质、不同含量的粮食CRM 进行检测试验,结果显示(表4),测定值与标准值的相对误差均在±10%范围内,符合GB/T32465—2015[10]规定的要求,且在标准值赋值范围内,表明该方法在准确度上有保证。上述结果也证明,在该方法下,2.1.4 所述消解液中的悬浮颗粒对镉元素提取及测定未产生明显影响。
表4 快速消解-标准加入法检测CRM 结果(n=7)
Table 4 Detection results of CRM using rapid digestion-standard addition (n=7)
CRM 名称 测定值/(mg/kg) 平均值/(mg/kg)标准值/(mg/kg) 相对误差/% RSD/%糙米粉 0.250 0.251 0.246 0.255 0.251 0.254 0.252 0.251 0.261±0.020 –3.8 1.2全麦粉 0.156 0.149 0.152 0.149 0.155 0.149 0.155 0.152 0.155±0.013 –1.9 2.1大米粉 0.172 0.182 0.172 0.182 0.179 0.180 0.176 0.178 0.180±0.020 –1.1 2.4
2.3.2 加标回收
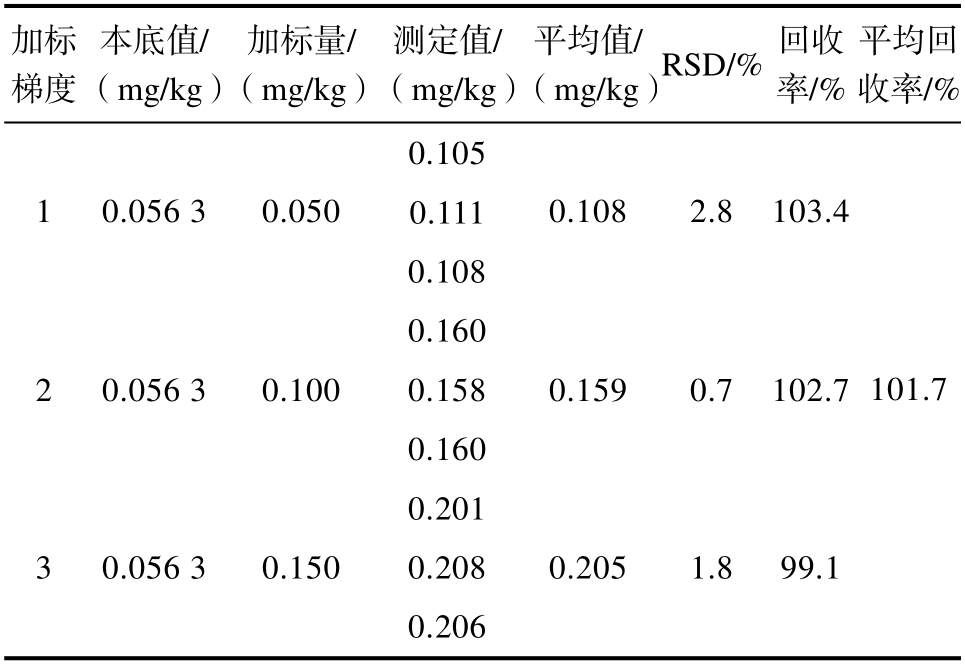
选择本底值较低的大米166#作为加标基质,进行低、中、高3 个梯度镉加标,各处理3 份平行样,每份样品上机重复测定3 次。结果见表5,3 个浓度水平的加标回收率为99.1%~103.4%,平均回收率为101.7%,符合GB/T 27404—2008[11]规定的回收率范围,表明该方法在低、中、高浓度镉检测上能保证相应的准确度。
表5 镉加标回收结果(n=3)
Table 5 Standard recoveries of cadmium (n=3)
加标梯度本底值/(mg/kg)加标量/(mg/kg)测定值/(mg/kg)(mg/kg)RSD/% 回收率/%平均值/平均回收率/%0.105 1 0.056 3 0.050 0.111 0.108 2.8 103.4 0.108 2 0.056 3 0.100 0.160 0.158 0.159 0.7 102.7101.7 0.160 3 0.056 3 0.150 0.201 0.208 0.205 1.8 99.1 0.206
2.3.3 方法精密度
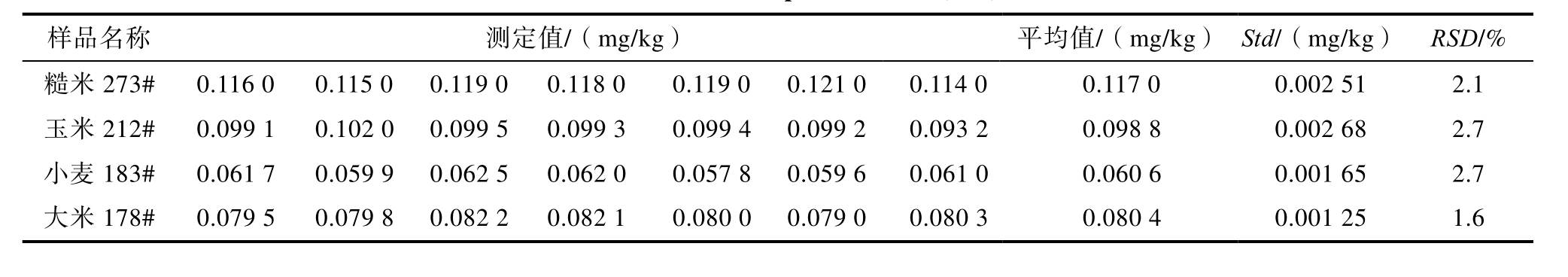
根据GB/T32465—2015[10]进行方法精密度研究。样品基质类型n= 4,每种基质检测m = 7 个子样,每个子样独立重复测定r = 3 次,共进行了d = 8 天试验,自由度为(n–1)m=21,优于精密度独立重复检测次数最低要求。根据表6,RSD 为1.6%~2.7%;结合表4,3 种CRM 的RSD 为1.2%~2.4%,标准物质样品与实际样品的RSD 值均小于3%,远低于11%的精密度期望值。上述结果表明,该方法对不同基质的粮食以及是否具有种皮的同种粮食,都显示出良好的精密度和方法重复性。
表6 精密度结果(n=7)
Table 6 Results of precision test (n=7)
平均值/(mg/kg) Std/(mg/kg) RSD/%0.117 0 0.002 51 2.1 0.098 8 0.002 68 2.7 0.060 6 0.001 65 2.7 0.080 4 0.001 25 1.6
2.4 方法检出限、方法空白
采用空白标准偏差的倍数法进行方法检出限评估。按照1.2.1 方法获得空白溶液,独立测定11次,得到标准偏差S 为0.011 7 µg/L,按照仪器检出限为3 S,计算得到仪器检出限IDL 为0.035 1 µg/L,带入方法公式计算方法检出限MDL 为0.003 mg/kg。按照定量限为10 S,计算方法定量限为0.01 mg/kg。本方法具有较低的试剂空白:≤0.05 µg/L(定容体积25 mL 时)。
2.5 与GB 5009.15—2014 微波消解-外标法比较
2.5.1 GB 5009.15—2014 检测结果
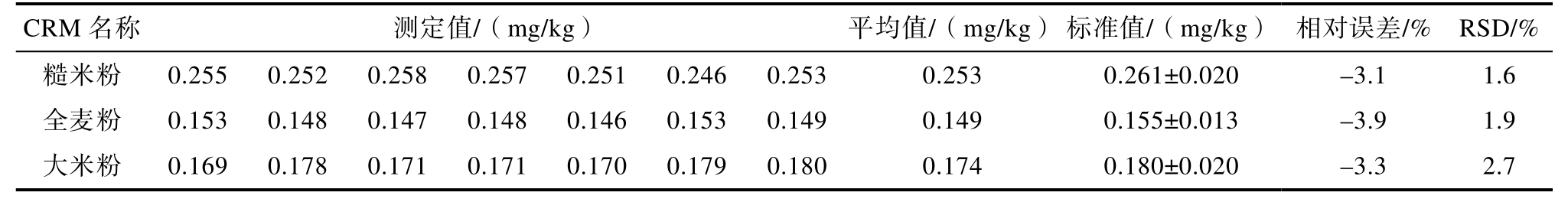
按照1.2.3 处理CRM 及实际样品,用外标法定量,原子吸收光谱仪检测,结果见表7~8。
表7 CRM 检测结果(n=7)
Table 7 Detection results of CRM (n=7)
CRM 名称 测定值/(mg/kg) 平均值/(mg/kg)糙米粉 0.255 0.252 0.258 0.257 0.251 0.246 0.253 0.253全麦粉 0.153 0.148 0.147 0.148 0.146 0.153 0.149 0.149大米粉 0.169 0.178 0.171 0.171 0.170 0.179 0.180 0.174标准值/(mg/kg) 相对误差/% RSD/%0.261±0.020 –3.1 1.6 0.155±0.013 –3.9 1.9 0.180±0.020 –3.3 2.7
表8 实际样品检测结果(n=7)
Table 8 Detection results of real samples (n=7)

样品名称 测定值/(mg/kg) 平均值/(mg/kg) Std/(mg/kg) RSD/%糙米273# 0.115 0 0.111 0 0.109 0 0.121 0 0.114 0 0.115 0 0.116 0 0.114 0 0.003 82 3.3玉米212# 0.098 6 0.101 0 0.099 5 0.096 8 0.098 0 0.107 0 0.097 3 0.099 7 0.003 49 3.5小麦183# 0.062 4 0.059 6 0.065 2 0.063 6 0.059 5 0.060 4 0.059 8 0.061 5 0.002 26 3.7大米178# 0.078 0 0.082 2 0.079 0 0.078 6 0.077 7 0.079 6 0.078 4 0.079 1 0.001 52 1.9
2.5.2 方法结果比对
根据表4~8 测定结果,对两种方法镉含量均值两两比对,进行F 检验及差异显著性检验(结果见表9)。当α = 0.05 时,F0.95(6、6)=4.28,F<F0.95(6、6),表明两种方法结果具有方差齐性,精密度一致。P > 0.05,表明两种方法均值无显著性差异,说明本文建立的快速消解–标准加入法,与国家标准方法GB 5009.15—2014 微波消解–外标法测定结果具有一致性。
表9 两种方法结果显著性检验(n=7)
Table 9 Results of significance test between the two methods (n=7)

国标方法本文方法 糙米粉CRM 全麦粉CRM 大米粉CRM 糙米273# 玉米212# 小麦183# 大米178#糙米粉CRM F=1.92 t=1.057 P=0.31全麦粉CRM F=1.30 t=1.873 P=0.09大米粉CRM F=1.22 t=1.471 P=0.17糙米273#F=2.33 t=1.489 P=0.16玉米212#F=1.71 t=0.558 P=0.59小麦183#F=1.88 t=0.852 P=0.41大米178#F=1.46 t=1.749 P=0.11
2.5.3 方法比较
根据两种样品前处理方法的试验研究结果,从十个方面进行比较(表10),本文方法(快速消解–标准加入法)与国标方法(微波消解–外标法)在准确性、精密度等方面无显著性差异,比国标方法节约时间88%,节省硝酸75%,所用仪器设备更少、价格更低。
表10 两种方法比较结果
Table 10 Results of the comparison between the two methods

序号 比较项目 方法1:本文方法 方法2:国标方法 比较结果1 前处理时间/min 25 202 方法1 比方法2 节约时间88%方法1 步骤少,更有利于避免样品污染或损失3 称样量/g 0.3~1(根据称样量改变硝酸量)2 前处理步骤 称样、加酸、消解、定容 消解罐泡酸、清洗烘干、称样、加酸、消解、转移、定容根据微波消解仪要求,0.3~0.5 方法1 可根据样品中镉含量调整称样量,高称样量提高检测准确性4 硝酸用量/mL 2.0 8.0 方法1 比方法2 节约硝酸75%,更经济环保5 消解温度/℃ 120 180 方法1 为中低温消解6 仪器设备 石墨赶酸器、原子吸收光谱仪方法2 前处理仪器昂贵,消解罐轮换慢,降低了处理效率7 准确性 标准值的96.2%~98.9% 标准值的96.1%~96.9% 都符合准确度要求,检测结果无显著性差异8 精密度/% 1.2~2.7 1.6~3.7 都符合要求,精密度一致9 方法检出限/(mg/kg) 0.003 0.001 处于同一数量级10 标准曲线线性 0.995~0.999 0.999 都满足准确定量要求微波消解仪、石墨赶酸器、原子吸收光谱仪
3 结论
本文建立了快速消解–标准加入法测定粮食中镉的方法,并与国家标准方法微波消解–外标法进行了全面比较。试验证实,采用68%硝酸作为消解液,优化样品与硝酸比例为0.3~0.4 g:2.0 mL,120 ℃消解15 min;按照样品基质不同分组,采用标准加入法进行标准曲线制作,标准曲线线性关系良好,且在4 种粮食基质中都显示出良好的适应性和稳定性。从方法性能指标看,该方法准确性高、精密度好、检出限低,与国家标准方法测定结果具有一致性,是一种准确的镉痕量测定方法;从效率和经济性方面看,该方法用时少、操作简便,前处理效率高,用酸量少、所需前处理仪器设备价格低,更加经济环保。该方法既保证了国家标准方法的准确度,又具有快速测定方法的高效率,是一种适用于大批量样品检测的高通量方法,在粮食质量日常监管、粮食清仓查库、食品安全应急快速检测中具有良好的应用前景。
[1] 食品安全国家标准食品中污染物限量: GB 2762—2017[S]. 北京: 中国标准出版社, 2017.National food safety standard Maximum levels of contaminants in foods: GB 2762—2017[S]. Beijing: Standards Press of China,2017.
[2] 食品安全国家标准食品中镉的测定: GB 5009. 15—2014[S].北京: 中国标准出版社, 2014.National food safety standard Determination of cadmium in foods: GB 5009. 15—2014[S]. Beijing: Standards Press of China, 2014.
[3] 吴云钊, 孟鹏, 曹民, 等. 不完全消解-石墨炉原子吸收光谱法测定粮食中的铅和镉[J]. 中国卫生检验杂志, 2014, 24(17):2464-2466.WU Y Z, MENG P, CAO M, et al. Determination of lead and cadmium in food stuff by using the method of incomplete digestion-graphite furnace atomic absorption spectrometry[J].Chinese Journal of Health Laboratory Technology, 2014, 24(17):2464-2466.
[4] 肖竹青, 袁丽红, 张华, 等. 直接提取进样石墨炉原子吸收法测定大米中的镉含量[J]. 粮油食品科技, 2016, 24(1): 61-63.XIAO Z Q, YUAN L H, ZHANG H, et al. Determination of cadmium content in rice by direct dilution injection graphite furnace atomic absorption spectrometry[J]. Science and Technology of Cereals, Oils and Foods, 2016, 24(1): 61-63.
[5] 刘坤. 利用湿法快速消解测定粮食中镉含量[J]. 粮食与饲料工业, 2017, 5: 62-64.LIU K. Rapid determination of cadmium in grain by wet digestion[J]. Cereal&feed industry, 2017, 5: 62-64.
[6] 唐懿, 李贵友, 杨微. 半消解悬浮液进样测定粮食样品中镉、铅、总砷含量[J]. 粮油食品科技, 2019, 27(2): 45-49.TANG Y, LI G Y, YANG W. Determination of cadmium, lead and total arsenic in grain samples by semi-digestion suspension injection[J]. Science and Technology of Cereals, Oils and Foods,2019, 27(2): 45-49.
[7] 数据的统计和解释正态分布均值和方差的估计与检验: GB/T 4889—2008 [S]. 北京: 中国标准出版社, 2008.Statistical interpretation of data—techniques of estimation and tests relating to means and variances of normal distribution:GB/T 4889—2008[S]. Beijing: Standards Press of China, 2008.
[8] 周明慧, 王松雪, 伍燕湘.稀酸温和提取直接进样快速测定大米中镉含量[J]. 中国粮油学报, 2015, 30(2): 97-102.ZHOU M H, WANG X S, WU Y X. Rapid direct sampling detection of Cd in rice using diluted acid extraction[J]. Journal of the Chinese Cereals and Oils Association, 2015, 30(2): 97-102.
[9] 张洁琼, 周明慧, 陈曦, 等. 谷物中多种元素测定的不完全消解快速前处理方法研究[J]. 分析试验室, 2019, 38(3): 355-359.ZHANG J Q, ZHOU M H, CHEN X, et al. Study on a rapid pretreatment of incomplete digestion to detect multielements in grain[J]. Chinese Journal of Analysis Laboratory, 2019, 38(3):355-359.
[10] 化学分析方法验证确认和内部质量控制要求: GB/T 32465—2015[S]. 北京: 中国标准出版社, 2015.Requirements for verification & validation of detection methods and internal quality control on chemical analysis:GB/T 32465—2015 [S]. Beijing: Standards Press of China, 2015.
[11] 实验室质量控制规范食品理化检测: GB/T27404—2008 [S].北京: 中国标准出版社, 2008.Criterion on quality control of laboratories—Chemical testing of food: GB/T27404—2008[S]. Beijing: Standards Press of China,2008.