表1 微波消解参数设定
高向阳1,高遒竹2,姚艳苹1
(1. 郑州科技学院 食品科学与工程学院,河南 郑州 450064; 2. 江南大学 食品学院,江苏 无锡 214122)
摘 要:为建立一种快速简便、准确测定食品中钙的新方法,选用坚果为样品,微波程序消解后,采用离子选择性电极加标浓度直读法测定钙含量。结果表明:钙电极的转换系数为98.61%,相对标准偏差均小于4%。该法测定简便快速、读数直观、成本低廉、样品用量少,为食品中钙的测定提供了一种全新的分析技术,有较强的创新性和推广应用价值。
关键词:微波消解;浓度直读法;钙;芝麻;花生;核桃
钙能维持神经和肌肉的兴奋,维持机体酸碱平衡,参与血凝过程,具有促进激素分泌、活化多种酶[1]和防控糖尿病[2]的重要作用。人体中钙含量不足或过剩均会影响机体的生长发育和健康[3]。严重缺钙时,婴幼儿会患佝偻病,中老年人易引起骨质和牙釉质疏松。人体补钙量过多时,会使婴幼儿骨骼过早钙化,影响生长发育,成年人易患结石症。因此,维持体内钙量的合理水平非常重要。
芝麻有滋补养生、软化血管、降低胆固醇的功效,可防止头发变白或脱落[4],延缓衰老[5-6]。花生仁含有儿茶素、蛋白质、维生素和多种微量元素,花生仁、核桃仁中所含卵磷脂和脑磷脂可防止细胞老化,增强记忆力[7],减少肠道对胆固醇的吸收,具有补气养血、通经益智、润肺润肠、润燥化痰等保健功能[8-9]。
目前,食品中钙的测定方法有火焰原子吸收光谱法[10]、电感耦合等离子体发射光谱法(ICP- AES)[11-12]、电感耦合等离子体质谱法(ICP- MS)[13]等。这些方法大多仪器昂贵、需配制标准溶液和作空白实验,操作繁琐耗时,计算复杂。浓度直读法所用仪器有断电保护和记忆功能,线性范围宽,无需作标准曲线。用两个标准溶液标定后测定试液,数分钟内可直接读取结果,已得到广泛应用[14-15]。但采用该法测定坚果中的钙尚未见文献报道,本文采用离子选择性电极加标浓度直读法测定坚果中的钙,所用仪器小巧便携、读数直观、测定快速,利于普及推广,为食品中钙的测定提供了一种新型分析技术。
芝麻、核桃:市售,购于郑州市超市;花生取自河南清丰县,自然风干。
无水氯化钙、氯化钾、氯化镁、磷酸二氢钠、磷酸氢二钠、浓盐酸、浓硝酸:郑州派尼化学试剂有限公司;氢氧化钠、三乙醇胺、30%双氧水:天津市致远化学试剂有限公司。所用试剂均为分析纯。水为饮用纯净水(电导率为2.56 μS/cm)。
钙离子标准储备溶液(10.00 g/L):准确称取经105 ℃干燥至恒重的无水氯化钙 2.776 5 g(精准至0.000 1 g)于50 mL小烧杯中,用水溶解并定容至100 mL。
钙离子标准溶液(100.00 mg/L):取1.00 mL钙离子标准储备液于100 mL容量瓶中,用水定容至100 mL。
三乙醇胺—盐酸缓冲剂和掩蔽剂(1.00 mol/L,pH 8.00):量取33.50 mL 99%的三乙醇胺于烧杯中,加浓盐酸20.85 mL,用氢氧化钾溶液调节pH至8.00后,用pH 8.00的水定容至250 mL。
三乙醇胺掩蔽剂(1.00 mol/L):取三乙醇胺14.00 mL于100 mL容量瓶中定容。
氯化钾(1.00 mol/L):称取7.448 5 g在120 ℃条件下干燥至恒重的氯化钾置于100 mL烧杯,少量水溶解后转移到100 mL容量瓶,用水定容。
钙离子A标定液(0.10 mg/L):用移液枪取100.00 mg/L钙离子标准溶液0.10 mL于小烧杯中,加入8.00 mL 1 mol/L氯化钾,用氢氧化钾调pH至8.00后,加入3.00 mL pH为8.00的三乙醇胺—盐酸缓冲溶液,移至100 mL容量瓶中,用pH为8.00的水定容。
钙离子B标定液(10.00 mg/L):取10.00 mL浓度为100.00 mg/L钙离子标准溶液于小烧杯中,加入8.00 mL 1 mol/L氯化钾,之后操作同钙离子A标定液。
钙离子空白溶液:取6.00 mL 1.00 mol/L氯化钾,用氢氧化钾调pH至8.00后,之后操作同钙离子A标定液。
101-1AS型电热鼓风干燥箱:北京市永光明医疗仪器有限公司;KQ5200DE型数控超声波清洗器:昆山市超声仪器有限公司;XT-9900A型智能微波消解仪、XT-9816-Ⅱ型样品前处理加热仪、XT-9700型冷却机:上海新拓分析仪器科技有限公司;雷磁pHS-3C型台式酸度计、雷磁PXSJ-216型离子分析仪、pCa-1钙选择性电极:上海仪电科学仪器股份有限公司。
样品用研钵研碎,置于恒重称量瓶中,于105 ℃干燥至恒质量。称取样品0.2 g左右(精准至0.000 1 g)分别放入溶样杯中,各加3 mL硝酸和1 mL 30%过氧化氢,放置过夜。按仪器说明书安装好溶样杯,按照表1设定的参数微波消解后,置于样品前处理加热仪上赶酸至溶液澄清,定量移入50 mL容量瓶定容,混匀,取10.00 mL于小烧杯中,添加100.00 mg/L钙离子标准溶液2.00 mL后,加入8.00 mL 1mol/L氯化钾,之后操作同钙离子A标定液,此为2.6等步骤的待测定试液。
表1 微波消解参数设定

按照雷磁PXSJ-216型离子分析仪说明书安装好仪器并预热15 min后,按“pX/9”键,再按“模式/4”键,选择“已知添加”测量模式;按“确认”键及“/0”或“/.”键,选择浓度单位“mg/L”;按两次“确认”键并选择“两点校准”,根据仪器提示输入A标定液的质量浓度值0.10 mg/L,并按下“确认”键。将清洗好的电极对和温度传感器插入A标定液中,轻晃烧杯10 s左右,待仪器电动势显示稳定后按“确认”键。再输入B标定液的浓度值10.00 mg/L,清洗好电极对并插入B标定液中。按照A标定液的相同操作标定B标定液,电动势显示稳定后按“确认”键,仪器自动给出校准后的电极斜率,按“确认”键,完成校准和标定。
仪器初始状态下按“模式/4”键,选择“已知添加”模式,按“确认”键后,选择浓度单位“mg/L”;按“确认”键,依次输入添加标液的体积值2.00 mL、试液的体积值100.00 mL、标液的浓度值100 mg/L,将清洗好的电极对及温度传感器插入待测液中,轻晃烧杯数秒后停止,待仪器电动势显示稳定后按“确认”键,直接显示试液中钙离子的质量浓度。干基样品中钙的质量分数计算公式为:
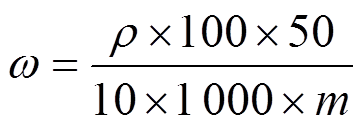
式中:ω,样品含钙的质量分数,mg/g;ρ,试液中钙离子的质量浓度,mg/L;m,称取的样品质量,g;100,测定时所用试液的体积,mL。
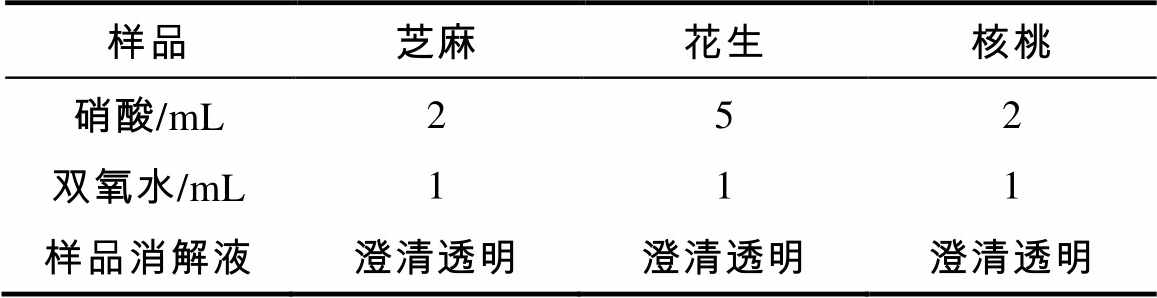
在智能微波消解仪的额定功率为1 000 W的条件下,对硝酸和双氧水消解剂用量进行单因素实验。结果表明:按表2设定的参数,消解效果较好。
表2 消解溶剂用量
转换系数是电极的实际响应斜率占理论斜率的百分比,其值越大,电极遵循能斯特方程的能力越高,是衡量电极质量的重要参数之一。按1.5方法对所用仪器进行校准和标定,25 ℃时钙离子选择性电极的理论斜率为29.580,用两点校准法测得所用钙电极的实际响应斜率为29.170,转换系数为98.61%,大于90%,表明所用电极有较好的能斯特响应[16]。
用1 000.00 mg/L的钙标准溶液,分别在pH为6.00、6.50、7.00、7.50、8.00、8.50、9.00时各进行3次平行测定,检验无可疑值后取平均值作图,结果见图1。
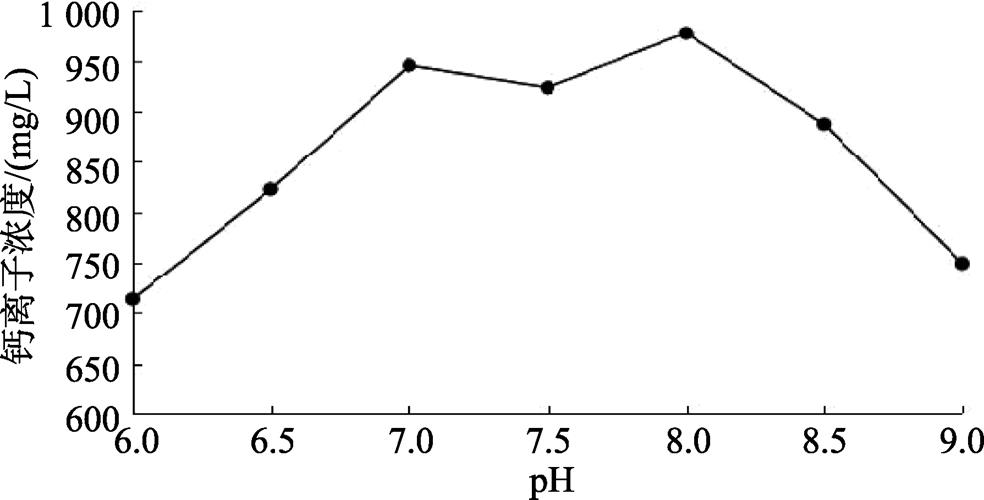
图1 pH值对钙离子浓度测定的影响
由图1可知,pH值为8.00时,测定信号较大,根据缓冲溶液的选择原则[17],确定pH 8.00为缓冲剂三乙醇胺—盐酸体系的最佳控制酸度。
在钙标准溶液浓度为1 000.00 mg/L、1.00 mol/L三乙醇胺—盐酸缓冲剂和掩蔽剂的pH为8.00的条件下,三乙醇胺—盐酸的加入量分别为0、1.00、2.00、3.00、4.00、5.00和6.00 mL时测定钙离子浓度,结果见图2。
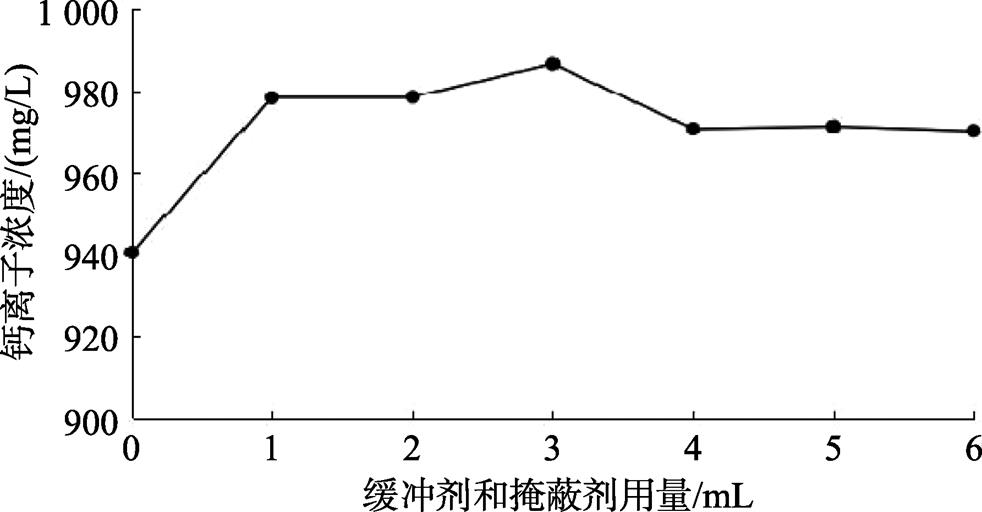
图2 缓冲剂和掩蔽剂用量对钙离子浓度测定的影响
由图2可知,缓冲剂和掩蔽剂的添加量为3.00 mL时,测定的准确度较高,因此选择1 mol/L三乙醇胺—盐酸(pH 8.00)的用量为3.00 mL。
三乙醇胺—盐酸(pH 8.00)用量3.00 mL时,分别添加2.00、4.00、6.00、8.00、10.00和12.00 mL的氯化钾(1.00 mol/L)到钙标准溶液(1 000.00 mg/L),测定钙离子浓度,结果见图3。
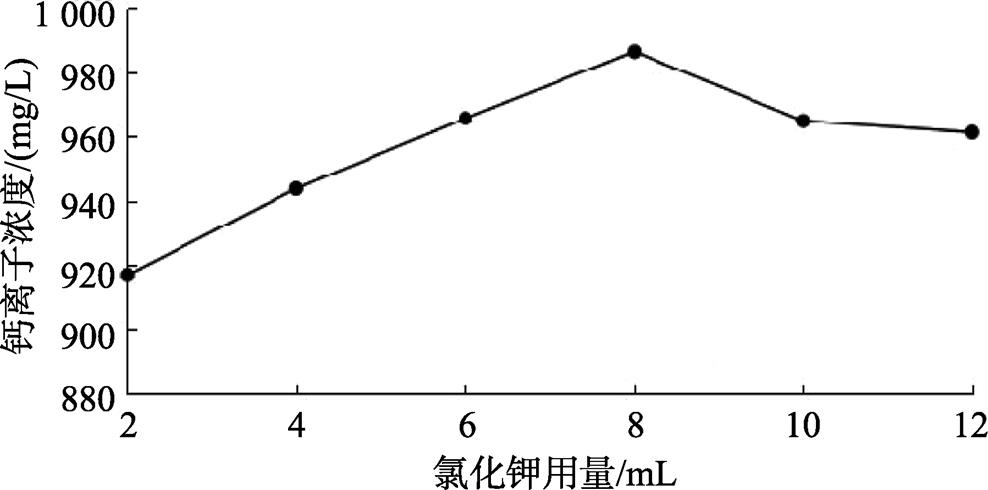
图3 氯化钾用量对钙离子浓度测定的影响
由图3可知,加入8.00 mL氯化钾时测定的误差最小。
取1.4定容的消解液10.00 mL于烧杯中,调节pH至8.00后转移到100 mL容量瓶中,加入三乙醇胺—盐酸3.00 mL,氯化钾8.00 mL,用pH 8.00的水定容,混匀。各样品按1.5步骤平行测定5次,检验无可疑值后取平均值,结果见表3。
表3 钙含量和精密度
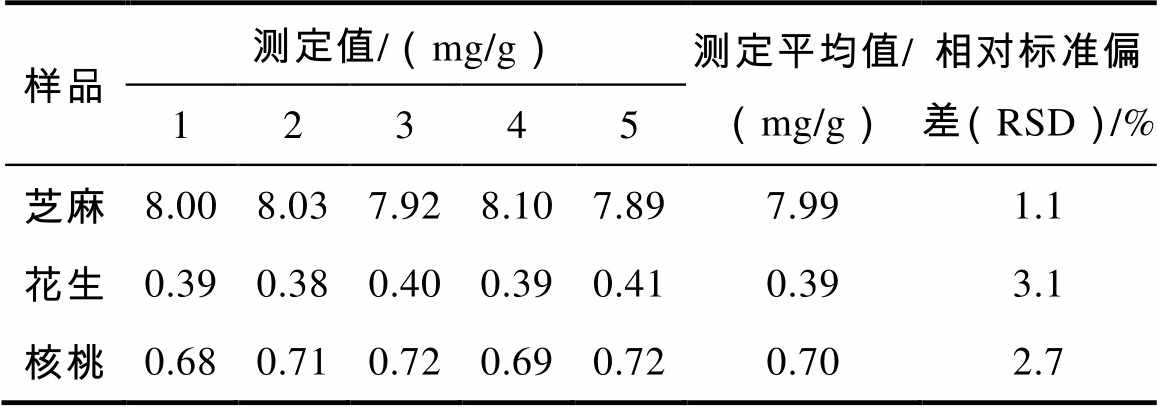
由表3可知,芝麻中钙含量为7.99 mg/g,花生中为0.39 mg/g,核桃中为0.70 mg/g,平行测定的RSD均小于4%。
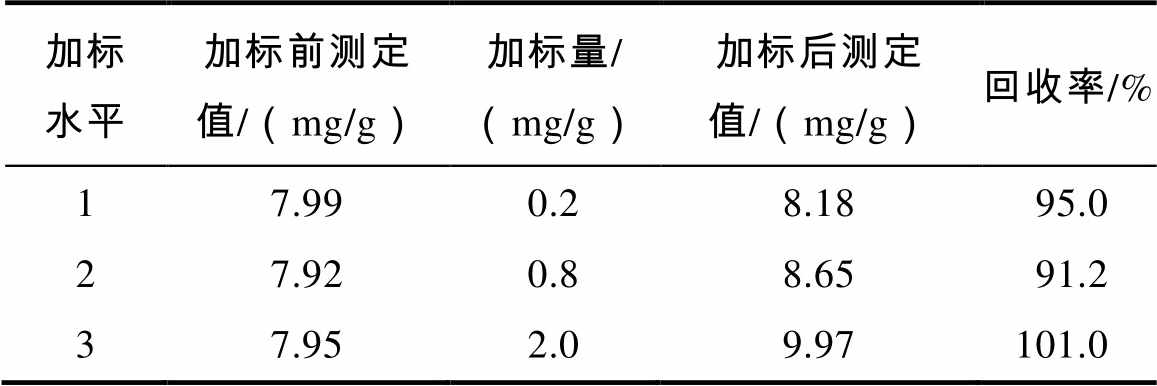
以芝麻为样品,分别取2.00、8.00、20.00 mL的100.00 mg/L钙标准溶液进行加标回收实验,每个加标水平平行测定3次,检验无可疑值后取平均值,结果如表4。
由表4可知,钙的加标回收率在91.2%~101.0%之间。
表4 钙回收率测定结果
以芝麻为样品,用加标浓度直读法和GB 5009.92—2016方法[18]对照测定,各进行5次平行测定,检验无可疑值后取平均值,结果如表5所示。
表5 对照测定数据
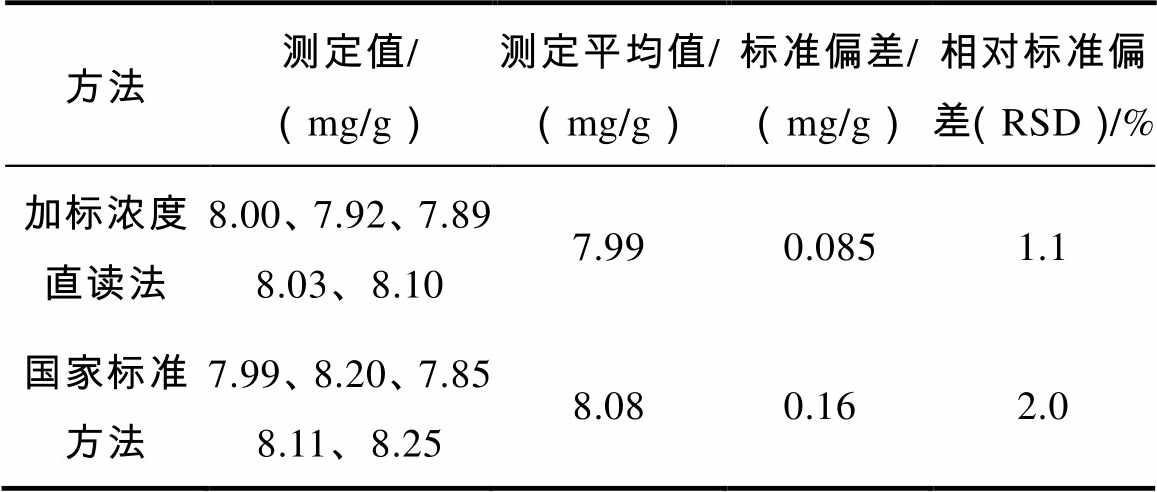
由表5可知,两种方法的标准偏差均小于0.2 mg/g,经F检验和T检验表明,在置信度为95%时,加标浓度直读法和GB 5009.92—2016方法测定的结果不存在显著性差异。
将微波消解技术和离子选择性电极加标浓度直读法有效结合,测定含油坚果中的钙。结果得出钙含量测定的最佳条件为:三乙醇胺—盐酸溶液pH为8.00,加入量3.00 mL,氯化钾溶液添加量8.00 mL。样品5次平行测定的RSD均小于4%,钙的回收率均在90%以上。该方法自动化程度高、选择性良好、试剂消耗量少、共存离子干扰少、测定简单快捷、读数直观、无需作标准曲线及进行繁琐的计算,且环境污染小,为坚果及其他油料类食品中钙含量的测定提供了一种较为理想的分析方法,有一定的推广应用价值和现实意义。
参考文献:
[1] 高向阳, 高遒竹. 微波消解—浓度直读法快速测定食品中微量钙的含量[J]. 食品安全质量检测学报, 2016, 7(8): 3061-3065.
[2] 郑飞飞, 范志红. 乳制品摄入与糖尿病风险防控[J]. 中国乳品工业, 2014, 42(6): 34-37.
[3] 魏新军. 食品营养与卫生学[M]. 北京: 中国农业科技出版社, 2001: 43-44.
[4] 沈梅. 黑芝麻和白芝麻微量元素含量的比较研究[J]. 中国卫生检验杂志, 2007, 17(12): 2309-2310.
[5] 沈旭丽. 芝麻的营养成分及保健价值[J]. 中国食物与营养, 2006, 7: 51-52.
[6] 梁国新. 黑芝麻的药用研究进展[J]. 中国老年保健医学, 2010, 8(5): 41-42.
[7] 赵志敏, 张潇风. 花生的保健功能及开发利用[J]. 中国食物与营养, 2007(7): 47-49.
[8] 朱冬, 王磊, 李超, 等. 核桃微量元素含量的测定[J]. 安徽农业科学, 2012, 40(16): 8947-8949.
[9] 黄黎慧, 黄群, 孙术国, 等. 核桃的营养保健功能与开发利用[J]. 粮食科技与经济, 2009(4): 48-50.
[10] 王锐, 刘仁春, 邓丽, 等. 火焰原子吸收光谱法测定苦刺花的微量元素[J]. 昭通学院学报, 2015, 37(5): 36-39.
[11] 叶润, 刘芳竹, 刘剑, 等. 微波消解-电感耦合等离子体发射光谱法测定大米中的铜、锰、铁、锌、钙、镁、钾、钠8种元素[J]. 食品科学, 2014, 35(6): 117-120.
[12] 代华均, 祝秀江, 尹庆红. 电感耦合等离子体发射光谱(ICP-AES)法测定橘子汁中钙和镁[J]. 中国无机分析化学, 2018, 8(1): 64-66.
[13] 樊祥, 曹晨, 张润何, 等. 全自动微波消解—电感耦合等离子体质谱法测定保健食品中12种常量、微量元素[J]. 分析试验室, 2018, 37(2): 157-162.
[14] 高向阳, 高遒竹, 王长青. 加标浓度直读法快速测定椒类调味品中的微量氟[J]. 中国调味品, 2016, 41(2): 116-120.
[15] 高向阳, 高遒竹, 张小燕, 等. 浓度直读法快速测定花生中氟含量及其分布[J]. 粮油食品科技, 2016, 24(1): 64-67.
[16] 高向阳. 新编仪器分析(第四版)[M]. 北京: 科学出版社, 2013: 150-151.
[17] 华中师范大学. 分析化学(第四版上册)[M]. 北京: 高等教育出版社, 2011: 166-168, 240-242.
[18] 食品中钙的测定: GB 5009.92—2016 [S].
Determination of calcium in sesame seeds, peanuts and walnuts by microwave digestion with standard addition direct reading method
GAO Xiang-yang1, GAO Qiu-zhu2, YAO Yan-ping1
(1. College of Food Science and Engineering, Zhengzhou Institute of Science and Technology, Zhengzhou Henan 450064; 2. College of Food Science and Technology, Jiangnan University, Wuxi Jiangsu 214122)
Abstract:A new, rapid, simple, accurate analysis method to detect calcium in foods was established. Some oily nuts were selected as samples, dissolved by microwave, and detected by ion selective electrode and standard concentration direct reading method. The results indicated that the conversion coefficient of calcium electrode was 98.61% and the relative standard deviation was less than 4%. The method is rapid, simple, direct reading, low cost and less sample consumption. It provides a new analytical technique for the determination of calcium in foods. The method has a strong creative and application value.
Key words:microwave digestion; concentration direct reading method; calcium; sesame seeds; peanuts; walnuts
DOI:10.16210/j.cnki.1007-7561.2018.06.010
中图分类号:TS 201.2+6;O 657.15
文献标识码:A
文章编号:1007-7561(2018)06-0049-05
收稿日期:2018-06-04
基金项目:郑州市科技局新兴产业研究与开发基金项目(153PXXCY186)
作者简介:高向阳,1949年出生,男,教授.