
杨秀军1,凌绍明2,欧阳辉祥2
(1.广西百色市粮油质量监督检验中心,广西 百色 533099;2.百色学院 化学与环境工程学院,广西 百色 533099)
摘 要:基于没食子酸丙酯与氯金酸还原反应生成的金纳米微粒在530 nm附近有最大吸收峰,建立一种用分光光度法测定食用油中没食子酸丙酯的新方法。探讨了氯金酸用量、加热温度和反应时间等因素对反应体系的影响,优化了试验条件,并对食用油中的共存物质进行了干扰试验。在最佳实验条件下,没食子酸丙酯的质量浓度在0.34~13.65 μg/mL范围内与纳米金粒子体系吸光度同试剂空白吸光度差值△A呈良好的线性关系,其回归方程为△A=0.160 3ρ+0.056 1,相关系数为0.994 6,检出限为0.093 μg/mL。该法用于食用油中没食子酸丙酯的测定,结果的RSD为0.9%~3.1%,平均回收率为90.3%~97.0%。
关键词:分光光度法;没食子酸丙酯;金纳米粒子;食用油
没食子酸丙酯(propyl gallate,PG)是一种优良的油脂和脂类食品的抗氧化剂,已被世界卫生组织(WTO)和联合国粮农组织(FAO)批准使用。由于其具有优良的耐热和抗氧化性能而被广泛应用于食品、药物、化妆品和饲料等领域,如PG能有效提高新资源食品——结构脂质(SLs)的氧化稳定性[1]。研究表明,过量使用PG会对人体的肾脏产生毒害作用[2],美国环境工作小组(EWG)于去年将PG列为12种“最脏”食品添加剂之一[3]。我国规定食品中添加的PG的最大使用量为0.2 g/kg。目前,检测PG的方法主要有高效液相色谱法[4-5]、液质联用法[6]、化学发光法[7]和光度法[8-9]等。研究发现,在pH7.0磷酸盐缓冲溶液及聚乙二醇存在下,PG与氯金酸作用生成纳米金微粒,体系在530 nm附件产生吸收,金纳米粒子体系的吸收变化量与PG的浓度具有良好的线性关系,建立光度法用于测定食用油中PG的含量。
1.1 主要仪器与试剂
UV-2700型紫外可见分光光度计:日本岛津公司;L6S型紫外可见光分光光度计:上海仪表电分析仪器有限公司;HH-S2数显恒温水浴锅:金坛市医疗仪器厂;BS124S电子分析天平:德国赛多利斯北京仪器公司。
PG标准溶液:准确称取0.025 6 g PG溶于适量石英亚沸二次蒸馏水,转入250 mL茶色容量瓶并定容至刻度,摇匀,于4℃冰箱保存备用,浓度为102.4 μg/mL;氯金酸储备液:取1.0 gHAuCl4·4H2O溶于适量石英亚沸二次蒸馏水配成100 mL储备液,于4℃储存,使用时稀释为167.39 μg/mL(以Au计,4℃储存);0.05%聚乙二醇(PEG20000)水溶液;磷酸氢二钠-磷酸二氢钠缓冲溶液(PBS):将0.2 mol/L的磷酸氢二钠和0.2 mol/L磷酸二氢钠溶液按一定比例混合得不同pH值得缓冲溶液;实验用试剂均为分析纯,试验用水为石英亚沸二次蒸馏水。
1.2 样品处理
样品的处理方法参照参考文献[10]。将称量好的20.00 g食用油(某品牌的花生油或调和油均购自广西百色市环球超市)溶于100mL石油醚中,超声10分钟后移入分液漏斗中,加入20 mL16.7 g/LCH3COONH4溶液,振荡2 min,静置出现分层后将水层放入另一个分液漏斗中(如果出现乳化现象,将乳化层一起排出),石油醚层分别用20 mL16.7 g/LCH3COONH4溶液进行两次抽提,然后每次用15 mL去离子水洗涤,重复两次,合并水层并静置。用滤纸过滤水层并转移至100 mL容量瓶中,将滤纸用少量去离子水洗涤,加入去离子水至刻度,摇匀。量取容量瓶中的溶液并用滤纸进行过滤,弃去约20 mL初滤液,过滤后的溶液保存待测。
1.3 实验方法
于5.0 mL具塞刻度试管中按一定的顺序加入700 μL PBS(pH7.0)、400 μL 167.39 μg/mL(以Au计)氯金酸水溶液、300 μL 0.05%PEG20000水溶液和一定量的PG标准溶液(或处理后待测样品试液),定容至3.0 mL后混匀,在50℃的恒温水浴锅中加热30 min,用自来水冷却至室温后,以石英亚沸蒸馏水做参比液,测定波长在530 nm处的吸光度A,同时测定相对应的空白试剂的吸光度Ab,计算△A=A-Ab值。
2.1 吸收光谱图
在磷酸盐缓冲溶液存在及PEG20000保护下,氯金酸与PG发生氧化还原反应生成酒红色纳米微粒金体系,体系在530 nm附近有吸收(见图1),随着PG用量的增加,生成的纳米金微粒越多,体系的吸收强度越大,并且发生蓝移。这是因为PG用量少时,生成的纳米金颗粒较大或发生微粒间聚集现象而导致蓝移[11]。故实验选择测定波长为530 nm。

图1 吸收光谱图
t=30 min,T=50℃,a-700 μLPBS+400 μLHAuCl4+300 μL0.05%PEG;b-a+10 μLPG;c-a+25 μLPG;d-a+50 μLPG;e-a+75 μLPG;f-a+100 μLPG
2.2 HAuCl4用量的影响
在700 μLPBS、300 μL0.05%PEG、100 μLPG以及反应温度50℃、反应时间30 min的条件下,试验考察了HAuCl4溶液用量对反应体系吸光度变化量ΔA的影响,结果见表1。
表1 氯金酸用量对体系的影响
氯金酸用量对体系影响较为显著。体系吸光度变化量ΔA值随着 HAuCl4溶液用量的增加而迅速增大,当氯金酸溶液用量为400 μL时ΔA值达到最大值,随后ΔA值随着氯金酸溶液用量的增加而减小。故实验选取氯金酸溶液的用量为400 μL。
2.3 缓冲溶液pH值及用量的影响
按实验方法对不同缓冲溶液pH值依次进行实验,结果发现缓冲溶液pH值为7.0时体系的ΔA较大而且稳定。实验对缓冲溶液用量进行了研究,结果表明缓冲溶液用量为700 μL时ΔA较大而且稳定。故实验选择缓冲溶液的pH值及用量分别为7.0和700 μL。
2.4 加热温度的影响
按照实验方法,考察了加热温度对反应体系吸光度变化量ΔA值的影响,结果见表2。
表2 反应温度的影响
反应体系吸光度变化量ΔA随着加热温度的增加而增大,加热温度为50℃时ΔA达到最大值,随后ΔA值随着加热温度的增加而减小。故实验选取的反应温度为50℃。
2.5 反应时间的影响
选择不同的加热时间进行实验,考察加热时间对反应体系吸光度变化量ΔA值的影响,结果见表3。
表3 反应时间的影响
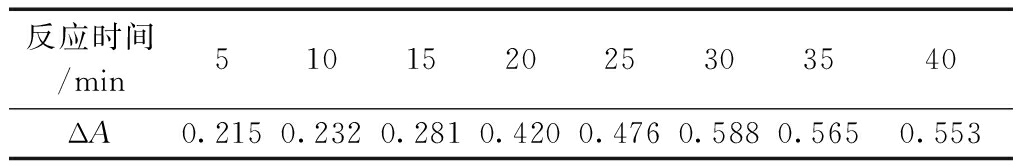
反应时间对体系的影响较为显著。实验发现,体系ΔA值随反应时间逐渐增加而增大,当反应时间为30 min时达到最大值,因此选定的反应时间是30 min。
2.6 线性方程及检出限
根据上述选定的实验条件,在PBS-HAuCl4-PEG反应体系中分别加入不同量的PG标准溶液到5.0 mL具塞试管中,用石英亚沸二次蒸馏水定容到3.0 mL,反应30 min后用自来水冷却,测定波长为530 nm处的吸光度A,以△A对PG标准溶液的浓度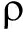 做工作曲线。结果表明,PG含量在0.34~13.65 μg/mL范围内与△A值呈线性关系,其线性回归方程为△A=0.160 3ρ+0.056 1,相关系数为0.994 6,检出限(3σ)是0.09 3 μg/L。
做工作曲线。结果表明,PG含量在0.34~13.65 μg/mL范围内与△A值呈线性关系,其线性回归方程为△A=0.160 3ρ+0.056 1,相关系数为0.994 6,检出限(3σ)是0.09 3 μg/L。
2.7 干扰物质影响实验
实验分析了干扰物质对反应体系的影响。当PG浓度为8.0 mg/L,相对误差在±5%之间时,下列倍数的离子不干扰测定:Na+(230),K+(120),Ba2+、Ca2+(100),Mn2+、Zn2+、Co2+、Mg2+(80),Cd2+、Cu2+(60),Fe2+(20),L-丙氨酸、L-精氨酸、L-缬氨酸(60),苯丙氨酸、DL-丝氨酸、苏氨酸、DL-谷氨酸、组氨酸(50),VB1(40)。由此可见,本法具有较好的选择性。
2.8 样品分析与不同方法比较
某品牌花生油和调和油购自于广西百色市环球超市。将处理好的样品试液按照1.3实验方法进行测定,分析结果见表4。
表4 食用调和油中PG的测定结果(n=5)
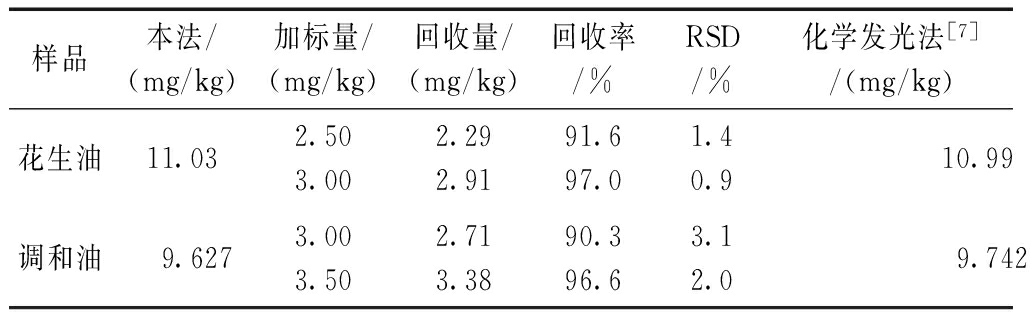
本法与化学发光法[7]的测定结果一致。
按照标准法[12]对实际样品进行分析,并与本法在操作步骤、线性范围、回收率和RSD%等方面进行比较,结果见表5。
表5 不同方法的比较结果
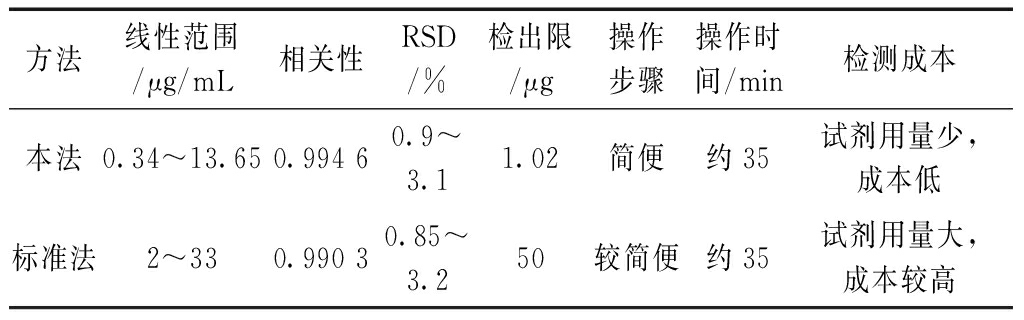
由表5可见,本法在线性范围、相关性、检出限和检测成本等方面具有一定的优势。
利用氯金酸与PG在一定条件下发生反应生成纳米金微粒,纳米金微粒体系在530 nm处有特征吸收峰,且PG的含量与纳米金体系吸光度变化值具有良好的线性关系,建立了一种分光光度法测定食用油中PG含量的方法。对影响测定PG含量的各种因素如氯金酸用量、反应温度和时间等因素进行研究。方法的线性回归方程为△A=0.160 3ρ+0.056 1,线性范围是0.34~13.65 μg/mL,相关系数为0.994 6,检出限为0.093 μg/mL。方法应用于食用油中PG含量测定,测定结果的RSD在0.9~3.1%,平均回收率在90.3~97.0%之间。本法操作简单、快捷,可应用于食用油中PG含量的测定。
参考文献:
[1]栾霞,王瑛瑶,郭咪咪,等.菜籽油和辛酸酶法合成结构脂质氧化稳定性的研究[J].粮油食品科技,2014,22(4):26-30.
[2]孟磊,谢黎霞,苏惠.反相高效液相色谱法测定儿童饼干中8种抗氧化剂[J].理化检验(化学分册),2013,49(10):1261-1263.
[3]食品伙伴网.美国环境工作小组(EWG)公布12种“最脏”食品添加剂[EB/OL].http://news.foodmate.net/2014/11/283674.html.[4]孟冬玲,刘畅,李小兰.离子液体双水相萃取-高效液相色谱法测定香精香料中的抗氧化剂[J].分析科学学报,2013,29(4):547-550.
[5]罗成玉,张耀明,王锋,等.高效液相色谱法测定食用植物油中5种抗氧化剂的含量[J].理化检验(化学分册),2011,47(6):687-689.
[6]张旭龙,刘银,巩治国,等.超高效液相色谱-串联质谱法同时测定聚合物食品包装材料中8种添加剂[J].色谱,2014,32(8):827-831.
[7]李丽,陈艳红,苏以申,等.高锰酸钾-甲醛-荧光素-没食子酸丙酯化学发光体系的研究[J],分析试验室,2012,31(12):66-68.[8]王萍,倪永年.抗氧化剂没食子酸丙酯合成纳米银及其应用[J].高等学校化学学报,2013,34(4):837-840.
[9]杜建中,姚媛,文超燕.高聚物萃取分光光度法测定茶多酚含量的研究[J].食品工业科技,2013,34(8):79-83.
[10]胡国华.食品添加剂应用基础[M].北京:化学工业出版社,2005:80-81.
[11]朱靖.贵金属纳米材料的绿色制备与表征[D].扬州:扬州大学,2009.
[13]GB/T 5009.32—2003,油脂中没食子酸丙酯(PG)的测定[S].![]()
YANG Xiu-jun1,LING Shao-ming2, OUYANG Hui-xiang2
(1.Baise Grain and Oil Quality Supervision and Inspection Center, Baise Guangxi 533099; 2.College of Chemical and Environmental Engineering, Baise University, Baise Guangxi 53300)
Abstract:A new method of determination of propyl gallate(PG) in cooking oil by spectrophotometry was developed, based on the principle of propyl gallate(PG) was reduced by chloroauric acid to produce gold nanoparticles, which had a strong absorption peak at 530nm.The effects of chloroauric acid concentration, heating temperature and reaction time on the systems, and interference test of coexisting substances in cooking oil were investigated, the conditions were optimized.Under the optimum experimental conditions, the concentration of PG was proportional to the △A in the range of 0.34~13.65 μg/mL.The linear equation was △A530nm=0.160 3ρ+0.056 1, with correlation coefficient was 0.994 6, and the detection limit was 0.093 μg/mL.The result of determine PG in cooking oil by the method was the RSD 0.9~3.1%, and the average recovery rate 90.3~97.0%.
Key words:spectrophotometry; propyl gallate; gold nanoparticles; cooking oil
收稿日期:2015-07-28
基金项目:桂西区域生态环境分析和污染控制广西高校重点实验室资助项目(桂教科研[2014]6号)
作者简介:杨秀军,1975年生,男,工程师,副主任.
通讯作者:凌绍明,1963年生,男,教授.
中图分类号:TS 207.3
文献标识码:A
文章编号:1007-7561(2016)02-0073-03